Foram encontradas 50 questões.
O etanol (C2H5OH), amplamente utilizado como combustível,
solvente industrial e componente de bebidas alcoólicas, tem suas
propriedades físico-químicas diretamente relacionadas aos tipos
de ligações e às interações entre suas moléculas. As ligações
intramolecular e intermolecular predominantes no etanol são,
respectivamente:
Provas
Questão presente nas seguintes provas
Em um processo no tratamento de efluentes industriais,
o dióxido de enxofre (SO2) é removido através da reação com
hidróxido de cálcio sólido, formando, então, sulfito de cálcio e
água, conforme a equação abaixo:
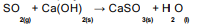
Sabendo que 32,0 g de dióxido de enxofre reagem completamente com excesso de hidróxido de cálcio, a massa (em gramas) de sulfito de cálcio (CaSO3) formada é:
Dados: S = 32 g mol–1 ; Ca = 40 g mol–1 ; O = 16 g mol–1 .
Sabendo que 32,0 g de dióxido de enxofre reagem completamente com excesso de hidróxido de cálcio, a massa (em gramas) de sulfito de cálcio (CaSO3) formada é:
Dados: S = 32 g mol–1 ; Ca = 40 g mol–1 ; O = 16 g mol–1 .
Provas
Questão presente nas seguintes provas
Durante uma análise em laboratório, um técnico em química
observa que uma amostra sólida é aquecida até derreter.
Em seguida, essa mesma amostra é dissolvida em água e,
posteriormente, reage com outra substância, formando, assim,
um novo produto. Com base nos fenômenos observados, podese afirmar que:
Provas
Questão presente nas seguintes provas
Uma célula galvânica utilizada para monitoramento de
corrosão consiste em um eletrodo de ferro (Fe²+/Fe) e um eletrodo
de prata (Ag+
/Ag), ambos operando em condições padrão.
Considerando o funcionamento espontâneo da célula, a diferença
de potencial padrão entre os dois eletrodos da célula em questão,
(E°), em volts, é igual a:
Dados:
E°(Fe²+ /Fe) = –0,44 V
E°(Ag+ /Ag) = +0,80 V
Dados:
E°(Fe²+ /Fe) = –0,44 V
E°(Ag+ /Ag) = +0,80 V
Provas
Questão presente nas seguintes provas
Um aluno deve selecionar corretamente dois condensadores
para diferentes sistemas de destilação. Enquanto o primeiro
sistema consiste em uma destilação simples de líquidos com
ponto de ebulição moderado, realizada à pressão atmosférica, o
segundo corresponde a um sistema de refluxo com aquecimento
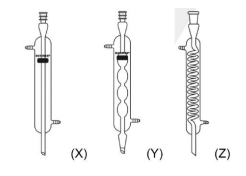
prolongado. Diante disso, e com base nas imagens (X), (Y) e (Z)
abaixo, pode-se afirmar que os condensadores escolhidos para o
primeiro e o segundo sistemas, respectivamente, foram:

Provas
Questão presente nas seguintes provas
A hemoglobina é uma proteína encontrada no interior das
hemácias, responsável pelo transporte de oxigênio (O2) no
sangue, e contém, em sua estrutura, o grupo heme, que apresenta
um íon ferro (Fe2+) coordenado por diferentes ligantes. A figura
abaixo mostra a estrutura química do grupo heme.
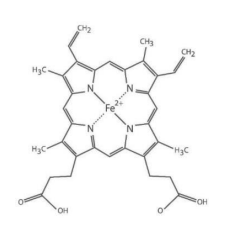
Considerando a química dos compostos de coordenação, pode-se afirmar que o transporte de O2 no organismo é prejudicado, em situações de intoxicação por monóxido de carbono (CO), pois o(a):

Considerando a química dos compostos de coordenação, pode-se afirmar que o transporte de O2 no organismo é prejudicado, em situações de intoxicação por monóxido de carbono (CO), pois o(a):
Provas
Questão presente nas seguintes provas
Pesquisadores de uma universidade estudam o aumento
da concentração média de um determinado gás em uma região
brasileira. Esse gás possui característica apolar com estrutura
linear, contribui para o aquecimento global, é produto da
combustão de combustíveis fósseis e participa diretamente do
ciclo biogeoquímico do carbono. O gás analisado e a sua principal
consequência ambiental são, respectivamente:
Provas
Questão presente nas seguintes provas
Os óxidos inorgânicos podem ser classificados de acordo
com seu comportamento ácido-base. Os óxidos básicos,
por exemplo, reagem com ácidos formando sal e água e, em
meio aquoso, formam bases. O composto que apresenta
exclusivamente um óxido básico é:
Provas
Questão presente nas seguintes provas
A eritromicina é um antibiótico macrolídeo amplamente
utilizado no tratamento de infecções bacterianas que tem sido
estudado em análises ambientais devido à sua presença como
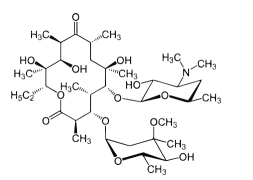
contaminante emergente em corpos d’água. Considerando a
sua estrutura química, apresentada a seguir, a massa molar da
eritromicina é:
Dados: C = 12 g mol–1 ; H = 1 g mol–1 ; N = 14 g mol–1 ; O = 16 g mol–1 .
Dados: C = 12 g mol–1 ; H = 1 g mol–1 ; N = 14 g mol–1 ; O = 16 g mol–1 .

Provas
Questão presente nas seguintes provas
Um técnico de laboratório constatou que, após uma aula de
Química Geral, resíduos de ácidos fortes, solventes orgânicos
e soluções contendo metais haviam sido descartados juntos,
em um mesmo recipiente, sem qualquer identificação e em
frasco inapropriado. Essa prática oferece risco à saúde e ao
meio ambiente. Diante da situação, e seguindo os princípios
da química verde, a conduta a ser adotada pelo técnico nas
próximas aulas será a de:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container