Foram encontradas 50 questões.
Texto I
Leia o texto abaixo e responda às questões 01, 02 e 03.
TEMPO
Quem teve a idéia de cortar o tempo em
fatias
foi um indivíduo genial.
5 fazendo-a funcionar no limite da exaustão.
entregar os pontos.
e tudo começa outra vez, com outro número
diferente.
Carlos Drummond de Andrade
No fragmento "...e tudo começa outra vez, com outro número", (verso 9) as palavras sublinhadas podem ser substituídas, sem que haja alteração de sentido, por:
Provas
Uma solução de ácido clorídrico foi preparada com 10,6 mL do reagente concentrado (1,19g/mL e 36%m/m) e água deionizada suficiente para preparar 250,00 mL de solução. A concentração aproximada da solução final é
Provas
O ácido cítrico (C6H8O7) reage com o hidróxido de sódio na proporção de 1:3. O volume aproximado de NaOH 0,300 mol/L gasto na neutralização de 25,00 mL de solução 0,92%m/v de ácido cítrico é
Provas
O volume de EDTA 0,0100 mol/L necessário para consumir 25,00 mL de uma solução contendo 750 mg CaCO3/L é
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
A Figura a seguir mostra a curva para a titulação de 50,00 mL de uma solução contendo cálcio com concentração 0,00500 mol/L pelo EDTA 0,0100 mol/L.
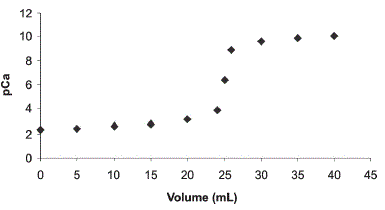
I. Nesta reação, a proporção estequiométrica entre o titulante e o titulado é de 1:1.
II. Nesta reação, o íon cálcio pode ser considerado como um ácido de Lewis, e o EDTA, como uma base de Lewis.
III. A concentração do íon complexo formado quando forem adicionados 25,00 mL de titulante é igual a 0,0500 mol/L.
IV. Para sinalizar o ponto final desta titulação, poder-se-ia utilizar um indicador que formasse um precipitado com o íon complexo no ponto estequiométrico.
V. A concentração do íon complexo formado quando forem adicionados 25,00 mL de titulante é igual a 0,00333 mol/ L.
Das afirmativas apresentadas estão corretas apenas
Provas
O tetrabarato de sódio, comumente conhecido como bórax (Na2B4O7.10H2O), é um padrão primário utilizado na padronização de soluções de ácido clorídrico, conforme mostra a reação abaixo:
Na2aB4O7 + 2 HCl + 5 H2O ⇌ 4 H3BO3 + 2 NaCl
Leia as afirmativas abaixo.
I. São necessários 23,825 g de bórax para se preparar 250,00 mL de solução padrão com concentração 0,250 mol/L.
II. São necessários 12,575 g de bórax para se preparar 250,00 mL de solução padrão com concentração 0,250 mol/L.
III. São necessários 11,25 mL de bórax 0,2000 mol/L para consumir 30,00 mL de solução de HCl 0,1500 mol/L.
IV. São necessários 22,50 mL de bórax 0,2000 mol/L para consumir 30,00 mL de solução de HCl 0,1500 mol/L.
V. São características indispensáveis de um padrão primário: ter alto peso molecular, não ser higroscópico e ser bastante solúvel.
Das afirmativas apresentadas, estão corretas apenas
Provas
Na determinação da pureza de uma amostra de cloreto do sódio (NaCl), foram gastos 18,00 mL de solução de AgNO3 com concentração 0,498 mol/L. Para tal, pesaram-se 0,552 g da amostra que foi totalmente solubilizada em um pequeno volume de água. A pureza dessa amostra é
Provas
O ácido acético (C2H4O2) apresenta as seguintes especificações: 1,049 g/mL e 99,78 mim. A concentração em mol/L do ácido concentrado é igual a
Provas
Uma solução tampão foi preparada pela mistura de 0,4 mols de um ácido fraco com 0,2 mols do sal da sua base conjugada. As afirmativas abaixo dizem respeito aesta solução.
I. O cálculo do pH desta solução seria através da expressão: pH=pKa+log[ácido fraco sal] / [ácido fraco]
II. A eficiência máxima desta solução se dará quando [sal]/ [ácido fraco] forigual a 1.
III. O cálculo do pH desta solução seria através da expressão: pH=pKa+log[ácido fraco]/[sal]
IV. A adição de uma pequena quantidade de água faz o pH desta solução aumentar.
V. A adição de uma pequena quantidade de água faz o pH desta solução diminuir.
Das afirmativas apresentadas, estão corretas somente
Provas
Considere os itens abaixo, sobre a utilização da internet:
I. Acessar sites de instituições financeiras por meio de endereços vindos em mensagens cujo remetente não seja conhecido.
II. Copiar arquivos da Internet e verificar se alguma legislação, em termos de direitos autorais, está sendo infringida.
III. Repassar correntes de e-mails somente se as informações forem comprovadamente verdadeiras.
IV. Preencher cadastros com informações pessoais somente em sites reconhecidamente seguros.
V. Não abrir o arquivo ao receber anexos não solicitados ou de destinatário desconhecido.
Das práticas de segurança apresentadas, estão corretas somente
Provas
Caderno Container