Foram encontradas 85 questões.
Foram adicionados 10 mL de solução aquosa de HCl em quatro béqueres contendo, respectivamente, pedaços de: (A)
magnésio (Mg), (B) alumínio (Al), (C) ferro (Fe) e (D) ouro (Au) metálicos, conforme esquema a seguir.

Provas
Questão presente nas seguintes provas
Sobre ligações químicas, considere as seguintes afirmativas:
I - A molécula de BF₃ contém um átomo com octeto incompleto. II - As moléculas PCl₅ e SiF₄ apresentam átomos de fósforo e enxofre com 12 elétrons e 10 elétrons na camada de valência, respectivamente. III - Algumas moléculas podem apresentar elétrons desemparelhados, tais como NO e ClO₂
Está correto o que se afirma em

I - A molécula de BF₃ contém um átomo com octeto incompleto. II - As moléculas PCl₅ e SiF₄ apresentam átomos de fósforo e enxofre com 12 elétrons e 10 elétrons na camada de valência, respectivamente. III - Algumas moléculas podem apresentar elétrons desemparelhados, tais como NO e ClO₂
Está correto o que se afirma em

Provas
Questão presente nas seguintes provas
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química CinéticaRepresentação das Transformações Químicas
Ligações do tipo iônica e covalente estão presentes na substância química representada pela fórmula:
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Técnicas de LaboratórioEquipamentos e Técnicas BásicasVidrarias
Um estudante de pós-graduação em Química Medicinal deseja fazer um experimento em cobaias de laboratório e
precisa preparar uma solução de cloridrato de metildopa. Ele deve administrar 100 mg a cada 6 horas nas cobaias. Para
tanto, ele precisa preparar uma solução aquosa de concentração comum igual a 50 g/L desse medicamento. Assinale a
alternativa que apresenta a vidraria indispensável para o preparo dessa solução.
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Uma solução de HCl foi padronizada empregando um padrão primário de Na₂CO₃ previamente seco em estufa por 24
horas a 110°C. Foi pesado 0,2500 g deste padrão primário e transferido para um erlenmeyer de 250 mL, sendo
dissolvidos com 50 mL de água destilada e adicionadas 3 gotas de indicador alaranjado de metila. Após colocar a solução
de HCl na bureta, efetuou-se a titulação, adicionando-se o ácido à solução de Na₂CO₃ até o ponto de viragem do
indicador, cor amarela. O volume de HCl consumido foi igual a 25,00 mL. Suponha que as pesagens do padrão primário e
as titulações foram feitas em triplicata e foram alcançados os mesmos valores nos três casos. Assinale a alternativa que
apresenta a concentração molar aproximada do HCl que deve ser encontrada após os cálculos.
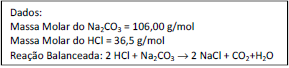
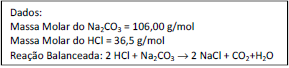
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Uma amostra de 25 mL de uma solução aquosa de H₂SO₄ foi titulada com uma solução aquosa 0,10 mol/L de KOH.
Determinou-se que o volume da base necessário para atingir a viragem do indicador foi igual a 20 mL. Suponha que as
titulações foram feitas em triplicata e todas forneceram os mesmos resultados. Assinale a concentração, em mol/L, de
H₂SO₄ na solução ácida.


Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Um técnico de laboratório possui uma solução-mãe de 0,10 mol/L de sacarose e deseja preparar 2 L de uma solução
diluída de concentração molar igual a 1 × 10⁻⁴ mol/L. O volume correto, em mililitros, a ser utilizado dessa solução-mãe
no preparo da nova solução, deverá ser igual a
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasPropriedades Coligativas: Tonoscopia, Ebulioscopia, Crioscopia e Pressão Osmótica.
A respeito do conceito de pressão de vapor, analise as seguintes situações.
I - Em uma cidade como Poços de Caldas, localizada a 1.196 metros acima do nível do mar, a temperatura de ebulição da água, em panela aberta, é superior a 100 °C como consequência da pressão atmosférica em Poços de Caldas ser maior que ao nível do mar. II - Na panela de pressão fechada, a água entra em ebulição acima de 100 °C graças à retenção de parte do vapor produzido, que gera aumento da pressão interna. III - Considerando três frascos iguais e fechados, numa mesma localidade, contendo volumes diferentes de água e todos mantidos à mesma temperatura, a pressão de vapor de água nos três frascos será a mesma em todos eles, desde que a quantidade de líquido colocada em cada um seja suficiente para que a quantidade de vapor formado atinja a pressão de vapor.
Está correto o que se afirma em
I - Em uma cidade como Poços de Caldas, localizada a 1.196 metros acima do nível do mar, a temperatura de ebulição da água, em panela aberta, é superior a 100 °C como consequência da pressão atmosférica em Poços de Caldas ser maior que ao nível do mar. II - Na panela de pressão fechada, a água entra em ebulição acima de 100 °C graças à retenção de parte do vapor produzido, que gera aumento da pressão interna. III - Considerando três frascos iguais e fechados, numa mesma localidade, contendo volumes diferentes de água e todos mantidos à mesma temperatura, a pressão de vapor de água nos três frascos será a mesma em todos eles, desde que a quantidade de líquido colocada em cada um seja suficiente para que a quantidade de vapor formado atinja a pressão de vapor.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
Sobre entalpia (H), assinale a afirmativa correta.
Provas
Questão presente nas seguintes provas
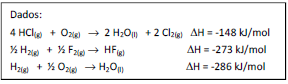
Dada a seguinte reação:
2 HCl(g) + F2(g) → 2 HF(g) + Cl2(g) ∆H = ?
Assinale a variação de entalpia, em kJ/mol, dessa reação.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container