Foram encontradas 60 questões.
A filtração é utilizada para a separação de misturas heterogêneas sólido-líquido. Qual o tipo de funil que é utilizado em conjunto com um sistema a vácuo para acelerar o processo de filtração?
Provas
Para contratação de um analista, uma empresa de alimentos submeteu os candidatos à análise de uma amostra de referência certificada (CRM) a qual continha 93 ± 1 g/kg de cálcio. Quatro candidatos foram avaliados, os quais realizaram 5 (cinco) réplicas em cada análise e obtiveram os seguintes resultados:
Candidato 1: 94, 92, 95, 98, e 100 g/kg.
Candidato 2: 92, 93, 94, 93 e 92 g/kg.
Candidato 3: 99, 91, 89, 97 e 90 g/kg.
Candidato 4: 98, 97, 96, 97 e 98 g/kg.
Em relação à exatidão e precisão das análises conduzidas pelos candidatos, é correto dizer que:
Provas
As análises baseadas em medidas de variação de massa são muito úteis em algumas técnicas analíticas, como a gravimetria, onde a pesagem correta e precisa é fundamental para garantir resultados confiáveis. Com relação aos fatores que causam erro na pesagem, quais das seguintes afirmativas são verdadeiras?
I. A eletrificação dos recipientes pode ocasionar erros na pesagem.
II. Os objetos a pesar devem estar na mesma temperatura da balança.
III. A umidade ambiente não influencia na pesagem.
IV. O deslocamento de ar durante a pesagem não influencia o resultado da pesagem.
Provas
Com base nos conceitos de erro sistemático e erro aleatório, avalie as afirmativas abaixo e selecione a opção que contém somente situações envolvendo erros sistemáticos.
I. O uso de um medidor de pH, calibrado incorretamente.
II.O erro produzido pelo ruído de um instrumento elétrico.
III. O uso de uma bureta descalibrada.
IV. O erro causado pelo descuido do analista em transferir um líquido de um recipiente para o outro.
Provas
Correlacione as vidrarias listadas na primeira coluna com as suas respectivas aplicações nas atividades laboratoriais listadas na segunda coluna. Qual é a sequência de números na segunda coluna que expressa a correlação correta?
1 – Bureta
2 – Funil de separação
3 – Pipeta volumétrica
4 – Balão volumétrico
5 – Kitassato
( ) Preparo de soluções com volume fixo e exato
( ) Filtração à vácuo
( ) Titulação volumétrica
( ) Extração líquido-líquido
( ) Transferência de volumes líquidos exatos
Provas
Em um experimento de destilação simples, a mistura a ser separada é aquecida e o vapor gerado é resfriado posteriormente. Qual é o nome do aparato utilizado para o resfriamento?
Provas
O gás carbônico produzido pelo corpo humano em uma aeronave espacial deve ser eliminado para a manutenção da vida dos tripulantes. Isso é feito reagindo o CO2 com hidróxido de sódio para formar água e carbonato de sódio, de acordo com a reação não balanceada abaixo:
!$ Na OH + CO_2 \rightarrow Na_2 CO_3 + H_2 O !$
Sabendo que um astronauta libera 1100 g de CO2 por dia, qual é a massa de hidróxido de sódio que deve ser carregada na aeronave para uma missão de exatamente 10 dias?
Dadas as massas molares: CO2 é 44 g . mol-1; NaOH é 40 g . mol-1;. Na2CO3 é 94 mol-1.
Provas
Após balancear as reações, abaixo, preenchendo as lacunas com os termos corretos (coeficiente estequiométrico e/ou composto químico), assinale a alternativa que contém a sequência dos termos que completa corretamente as lacunas.
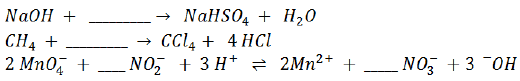
Provas
O composto de cianamida de cálcio é preparado em quantidades apreciáveis para ser utilizado como fertilizante sólido. O reagente sólido é misturado ao solo e reage lentamente com a água liberando amônia e carbonato de cálcio no solo, segundo a reação abaixo:
Marque a opção que corresponde à massa (em kg) de amônia produzida a partir de 200 kg de cianamida de cálcio. Dadas as massas molares: CaCN2 = 80 g . mol-1; CaCO3 = 100 g . mol-1; H2O = 18 g . mol-1; NH3 = 17 g . mol-1.
Provas
O monóxido de nitrogênio (óxido nítrico) é um poluente gasoso liberado no ar pela combustão de motores de automóveis. Quando reage com oxigênio, produz o dióxido de nitrogênio, um gás castanho amarelado, irritante ao trato respiratório e aos olhos. A equação da reação, não balanceada, é a seguinte:
!$ NO_(g) + O_{2(g)} \rightarrow NO_{2(g)} !$
Supondo que 120 gramas de NO reajam com um excesso de oxigênio, quantos mols de dióxido de nitrogênio serão produzidos?
Dadas as massas molares: NO = 30 g . mol-1; NO2 = 46 g . mol-1; O2 = 32 g . mol-1.
Provas
Caderno Container