Foram encontradas 351 questões.
Industrialmente, o gás hélio é obtido a partir da condensação fracionada dos componentes do gás natural. Embora encontrado em pequena proporção na atmosfera terrestre, o hélio é o segundo elemento químico em abundância no universo. Elepode ser formado a partir de reações de fusão de isótopos de hidrogênio, as quais são altamente exotérmicas e são a principal fonte de energia do Sol. Uma dessas reações é mostrada na equação abaixo, em que o índice superior corresponde ao número de massa da espécie e o inferior, ao número de prótons. A equação mostra, ainda, a variação de entalpia ( !$ \Delta H !$ ) da reação.
!$ _1^2H + _1^?H \rightarrow _2^4H + _0^1n \quad \Delta H = 1,5 \times 10^{12} \ {J \over \text{mol}} !$
Até o momento, não existe tecnologia suficiente para controlar as reações de fusão nuclear e, dessa forma, não se consegue empregá-las como fonte de energia.
Tendo o texto acima como referência inicial, julgue o item.
Considere que, em termos da porcentagem de volume, uma amostra de gás natural bruto seja composta por 1,0% de He, 90,0% de CH4 e 9,0% de CO2. Nesse caso, para essa amostra, considerando-se o comportamento ideal para o gás natural, a concentração de He, em porcentagem de massa, é superior a 1,0%.
Provas
O nitrometano — CH3NO2 — é frequentemente usado como aditivo em combustíveis para aeromodelos e veículos de competição. Em decorrência do elevado teor de oxigênio do composto, é necessário menos O2 (g) durante a sua combustão, o que permite a injeção de maior quantidade de combustível no motor e resulta em ganho de potência.
Considerando o texto acima e sabendo que a fórmula molecular do octano, componente típico da gasolina, é C8H18, assinale a opção correta.
Assinale a opção que mostra uma estrutura correta da molécula de nitrometano.
Provas
O nitrometano — CH3NO2 — é frequentemente usado como aditivo em combustíveis para aeromodelos e veículos de competição. Em decorrência do elevado teor de oxigênio do composto, é necessário menos O2 (g) durante a sua combustão, o que permite a injeção de maior quantidade de combustível no motor e resulta em ganho de potência.
Considerando o texto acima e sabendo que a fórmula molecular do octano, componente típico da gasolina, é C8H18, julgue o item.
A combustão nos motores a gasolina é comparável ao metabolismo aeróbio de uma célula pelo fato de que ambos associam um combustível ao oxigênio molecular e os transformam em CO2 e H2O (e outros produtos, conforme o caso), com aproveitamento parcial da energia liberada nas reações.
Provas
O nitrometano — CH3NO2 — é frequentemente usado como aditivo em combustíveis para aeromodelos e veículos de competição. Em decorrência do elevado teor de oxigênio do composto, é necessário menos O2 (g) durante a sua combustão, o que permite a injeção de maior quantidade de combustível no motor e resulta em ganho de potência.
Considerando o texto acima e sabendo que a fórmula molecular do octano, componente típico da gasolina, é C8H18, julgue o item.
O nitrometano é um isômero da metanamida.
Provas
A partir de 2014, passou a ser disputado o campeonato mundial de Fórmula E, categoria de automobilismo em que os veículos são movidos a eletricidade. No primeiro ano, todos os veículos utilizaram baterias de íon-lítio, com potência máxima de 200 kW. Os carros foram dotados de um sistema de armazenamento e recarga de energia, que transforma a energia cinética do carro em carga para a bateria.
As principais vantagens das baterias de íon-lítio são a elevada tensão elétrica gerada (da ordem de 4,0 V) e a elevada densidade energética (entre 100 e 150 Wh/kg). O funcionamento das baterias se baseia na migração de íons Li+ através de um eletrólito. Em uma das configurações mais comuns, o anodo é um eletrodo de carbono, enquanto o catodo é formado por LiCoO2. No processo de carga, o anodo de carbono é abastecido com elétrons vindos do catodo e, para que a neutralidade seja mantida, íons Li+ migram simultaneamente do catodo para o anodo. Na descarga, o processo se inverte: os elétrons migram do anodo para o catodo através do circuito externo, gerando a corrente elétrica. As reações podem ser indicadas conforme a equação a seguir.
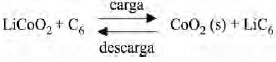
Internet: <www.jmbatterysystems.com> (com adaptações).
Tendo como referência inicial as informações acima, julgue o item.
Considere que uma equipe tenha feito as seguintes observações relativas ao desempenho de seus veículos em determinada temporada: na primeira corrida, o desempenho foi 1% superior ao da temporada anterior; a cada corrida, o desempenho foi melhorando 1% com relação à corrida anterior. Nessa situação, considerando-se 1,105 como valor aproximado para 1,0110, infere-se que, na 20.ª corrida da temporada, a melhoria no desempenho dos veículos ainda não teria atingido 22% em relação à temporada anterior.
Provas
A partir de 2014, passou a ser disputado o campeonato mundial de Fórmula E, categoria de automobilismo em que os veículos são movidos a eletricidade. No primeiro ano, todos os veículos utilizaram baterias de íon-lítio, com potência máxima de 200 kW. Os carros foram dotados de um sistema de armazenamento e recarga de energia, que transforma a energia cinética do carro em carga para a bateria.
As principais vantagens das baterias de íon-lítio são a elevada tensão elétrica gerada (da ordem de 4,0 V) e a elevada densidade energética (entre 100 e 150 Wh/kg). O funcionamento das baterias se baseia na migração de íons Li+ através de um eletrólito. Em uma das configurações mais comuns, o anodo é um eletrodo de carbono, enquanto o catodo é formado por LiCoO2. No processo de carga, o anodo de carbono é abastecido com elétrons vindos do catodo e, para que a neutralidade seja mantida, íons Li+ migram simultaneamente do catodo para o anodo. Na descarga, o processo se inverte: os elétrons migram do anodo para o catodo através do circuito externo, gerando a corrente elétrica. As reações podem ser indicadas conforme a equação a seguir.

Internet: <www.jmbatterysystems.com> (com adaptações).
Tendo como referência inicial as informações acima, julgue o item.
Considere que dois veículos (A e B) realizarão uma corrida de 64 voltas, em uma pista fechada com 4,1 km de extensão. Considere, ainda, que durante a corrida os veículos se desloquem com velocidade escalar constante e que A dê uma volta completa na pista em 80 s e B gaste 2 s a mais para percorrer a mesma distância. Nessa situação, se, na largada, A estiver 20 m à frente de B, então, antes da metade da corrida, A estará uma volta completa na frente de B.
Provas
A partir de 2014, passou a ser disputado o campeonato mundial de Fórmula E, categoria de automobilismo em que os veículos são movidos a eletricidade. No primeiro ano, todos os veículos utilizaram baterias de íon-lítio, com potência máxima de 200 kW. Os carros foram dotados de um sistema de armazenamento e recarga de energia, que transforma a energia cinética do carro em carga para a bateria.
As principais vantagens das baterias de íon-lítio são a elevada tensão elétrica gerada (da ordem de 4,0 V) e a elevada densidade energética (entre 100 e 150 Wh/kg). O funcionamento das baterias se baseia na migração de íons Li+ através de um eletrólito. Em uma das configurações mais comuns, o anodo é um eletrodo de carbono, enquanto o catodo é formado por LiCoO2. No processo de carga, o anodo de carbono é abastecido com elétrons vindos do catodo e, para que a neutralidade seja mantida, íons Li+ migram simultaneamente do catodo para o anodo. Na descarga, o processo se inverte: os elétrons migram do anodo para o catodo através do circuito externo, gerando a corrente elétrica. As reações podem ser indicadas conforme a equação a seguir.

Internet: <www.jmbatterysystems.com> (com adaptações).
Tendo como referência inicial as informações acima, julgue o item.
Considere a reação global a seguir, que ocorre nas baterias convencionais chumbo/ácido e os potenciais padrões das semirreações (Eº) fornecidos na tabela.
PbO2(s) + Pb(s) + 2SO42-(aq) + 4H+ (aq) → 2PbSO4 + 2H2O
|
semirreação |
Eº (V) |
|
PbSO4 + 2e- → Pb + SO42- |
-0,36 |
|
PbO2 + SO42- + 4H+ + 2e- → PbSO4 + 2H2O |
1,69 |
A partir dessas informações, conclui-se que é necessária a conexão em série de pelo menos duas baterias chumbo/ácido, operando sob condições padrão, para que seja gerado um potencial elétrico igual ou superior a 4,0 V.
Provas
A partir de 2014, passou a ser disputado o campeonato mundial de Fórmula E, categoria de automobilismo em que os veículos são movidos a eletricidade. No primeiro ano, todos os veículos utilizaram baterias de íon-lítio, com potência máxima de 200 kW. Os carros foram dotados de um sistema de armazenamento e recarga de energia, que transforma a energia cinética do carro em carga para a bateria.
As principais vantagens das baterias de íon-lítio são a elevada tensão elétrica gerada (da ordem de 4,0 V) e a elevada densidade energética (entre 100 e 150 Wh/kg). O funcionamento das baterias se baseia na migração de íons Li+ através de um eletrólito. Em uma das configurações mais comuns, o anodo é um eletrodo de carbono, enquanto o catodo é formado por LiCoO2. No processo de carga, o anodo de carbono é abastecido com elétrons vindos do catodo e, para que a neutralidade seja mantida, íons Li+ migram simultaneamente do catodo para o anodo. Na descarga, o processo se inverte: os elétrons migram do anodo para o catodo através do circuito externo, gerando a corrente elétrica. As reações podem ser indicadas conforme a equação a seguir.

Internet: <www.jmbatterysystems.com> (com adaptações).
Tendo como referência inicial as informações acima, julgue o item.
Considerando-se que a massa molar do lítio seja 6,9 g/mol e que a constante de Faraday seja 96.500 C/mol, conclui-se que, se uma bateria íon-lítio operar durante 9.650 s com intensidade de corrente elétrica constante e igual a 2,0 A, então a quantidade de íons lítio transferida durante essa operação será superior a 1,0 g.
Provas
A partir de 2014, passou a ser disputado o campeonato mundial de Fórmula E, categoria de automobilismo em que os veículos são movidos a eletricidade. No primeiro ano, todos os veículos utilizaram baterias de íon-lítio, com potência máxima de 200 kW. Os carros foram dotados de um sistema de armazenamento e recarga de energia, que transforma a energia cinética do carro em carga para a bateria.
As principais vantagens das baterias de íon-lítio são a elevada tensão elétrica gerada (da ordem de 4,0 V) e a elevada densidade energética (entre 100 e 150 Wh/kg). O funcionamento das baterias se baseia na migração de íons Li+ através de um eletrólito. Em uma das configurações mais comuns, o anodo é um eletrodo de carbono, enquanto o catodo é formado por LiCoO2. No processo de carga, o anodo de carbono é abastecido com elétrons vindos do catodo e, para que a neutralidade seja mantida, íons Li+ migram simultaneamente do catodo para o anodo. Na descarga, o processo se inverte: os elétrons migram do anodo para o catodo através do circuito externo, gerando a corrente elétrica. As reações podem ser indicadas conforme a equação a seguir.

Internet: <www.jmbatterysystems.com> (com adaptações).
Tendo como referência inicial as informações acima, julgue o item.
Mesmo oferecendo menos riscos ao ambiente que as baterias de mercúrio, as baterias de íon-lítio devem ser recicladas, assim como as de mercúrio.
Provas
A partir de 2014, passou a ser disputado o campeonato mundial de Fórmula E, categoria de automobilismo em que os veículos são movidos a eletricidade. No primeiro ano, todos os veículos utilizaram baterias de íon-lítio, com potência máxima de 200 kW. Os carros foram dotados de um sistema de armazenamento e recarga de energia, que transforma a energia cinética do carro em carga para a bateria.
As principais vantagens das baterias de íon-lítio são a elevada tensão elétrica gerada (da ordem de 4,0 V) e a elevada densidade energética (entre 100 e 150 Wh/kg). O funcionamento das baterias se baseia na migração de íons Li+ através de um eletrólito. Em uma das configurações mais comuns, o anodo é um eletrodo de carbono, enquanto o catodo é formado por LiCoO2. No processo de carga, o anodo de carbono é abastecido com elétrons vindos do catodo e, para que a neutralidade seja mantida, íons Li+ migram simultaneamente do catodo para o anodo. Na descarga, o processo se inverte: os elétrons migram do anodo para o catodo através do circuito externo, gerando a corrente elétrica. As reações podem ser indicadas conforme a equação a seguir.

Internet: <www.jmbatterysystems.com> (com adaptações).
Tendo como referência inicial as informações acima, julgue o item.
No processo de carga da bateria íon-lítio, o cobalto é oxidado do estado Co3+ para Co4+.
Provas
Caderno Container