Foram encontradas 35.978 questões.
Os íons X+ e A- são isoeletrônicos do gás nobre argônio.
O elemento que dá origem ao _________________ íon X+ pertence ao período da Classificação Periódica e apresenta _________________ prótons. O elemento representado por A é o _________________ .
As lacunas são preenchidas, correta e respectivamente, por
Provas
Na cocção de alimentos à base de carne bovina, ocorre a liberação de uma substância composta apenas por carbono, hidrogênio e oxigênio. Quando 1,0 mol desta substância é analisada por combustão completa forma-se 2 mol de moléculas de água e 3 mol de dióxido de carbono. A massa de oxigênio desta molécula corresponde a 4 vezes a massa de hidrogênio existente em 1 mol dessa substância.
A fórmula mínima dessa substância é
Provas
O Brasil é o maior produtor mundial de nióbio, um metal estratégico utilizado em diversas indústrias, como a siderúrgica, aeroespacial e de alta tecnologia. Uma de suas aplicações é em sensores e lasers de niobato de lítio, composto que contém em sua fórmula unitária um íon Li+ e o oxiânion formado pelo nióbio no estado de oxidação +5.
O número de átomos de oxigênio por fórmula unitário do niobato de lítio é
Provas
A curva de aquecimento de uma substância pura é apresentada na figura.
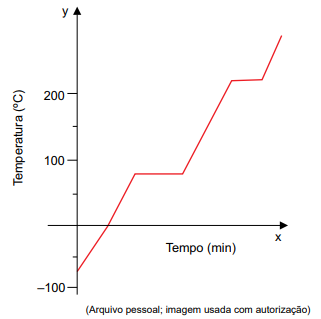
A tabela apresenta dados de temperatura de fusão e ebulição (em kelvin) de algumas substâncias.
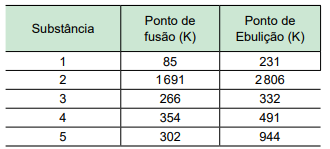
A curva de aquecimento da figura é compatível com a substância de número
Provas
Um litro de uma solução aquosa apresenta a composição iônica apresentada na figura.
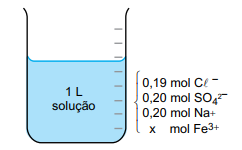
A quantidade x, em mol, de íons de Ferro3+ é
Provas
Os combustíveis produzidos a partir de fontes renováveis desempenham um papel importante na matriz energética brasileira.
Dentre eles, o mais amplamente utilizado no Brasil e sua principal fonte de produção é o
Provas
Provas
Os dados da tabela referem-se a experimentos cinéticos envolvendo reagentes e medidas de rapidez da reação representada genericamente por

A partir dos dados da tabela, determina-se que a ordem global da reação representada na equação é
Provas
O seleneto de mercúrio (II) (HgSe) é usado na fabricação de detectores de infravermelho e em tecnologias relacionadas a sensores térmicos. A sua obtenção é feita a partir da reação entre o cloreto de mercúrio (II) (HgCl2) e o dióxido de selênio (SeO2), de acordo com a equação a seguir.
HgCl2 (s) + NaCN (aq) + NH4 OH (aq) + SeO2 (s) + SO2 (g)
HgSe (s) + NaCl (aq) + NH4 CN (aq) + (NH4)2SO4 (aq) + H2 O (l)
Para a formação de 1 mol de HgSe, a quantidade em mol de elétrons envolvidos no processo e a soma dos coeficientes estequiométricos dos reagentes dessa reação são, respectivamente,
Provas
Um gás, contido em um cilindro a 27 º C e 2,1 atm apresenta densidade igual a 3,5 g/L.
Considerando R = 0,08 atm⋅L⋅mol–1 K–1 , calcula-se que o gás é o
Provas
Caderno Container