Foram encontradas 36.167 questões.
Acerca de polímeros, julgue os itens a seguir.
I As pontes de dissulfeto diminuem a durabilidade da borracha vulcanizada.
II Elastômeros são materiais que, depois de serem esticados, voltam à sua forma original.
III Os elastômetros são polímeros conhecidos como borracha sintética devido à sua completa diferença estrutural com a borracha natural.
IV Pneus de automóveis são feitos de borracha vulcanizada, o que garante sua resistência a agentes químicos e ao calor.
Estão certos apenas os itens
Provas
O polipropileno, cuja fórmula estrutural está apresentada a seguir, é formado por um único tipo de monômero de cadeia carbônica insaturada, por isso é classificado como polímero de adição. Sua aplicação é muito diversificada, sendo empregado, por exemplo, na confecção de cordas, de pente de cabelo, de copos, de botões de roupa etc.
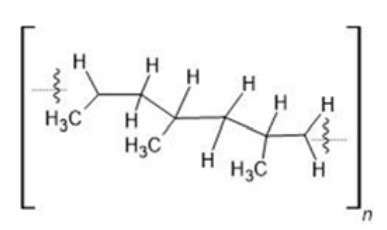
Considerando as informações anteriores, assinale a opção que corresponde à estrutura do monômero capaz de formar o polipropileno.
Provas
O petróleo é originado de fósseis subterrâneos. Após sua extração do subsolo, ele é transportado para as refinarias, onde passa por um processamento para separação das frações de compostos de acordo com as massas moleculares. A gasolina, fabricada a partir do petróleo, é uma mistura de hidrocarbonetos que têm de 6 a 10 átomos de carbono.
A partir das informações precedentes, assinale a opção correta.
Provas
As cadeias carbônicas podem ser representadas na forma condensada, como em I, em que não se destacam os traços que representam as ligações entre os átomos; na forma de traços ou zigue-zague, como em II, que se aproxima mais do modelo real da cadeia carbônica, por considerar os ângulos das ligações entre os átomos; ou na forma estendida, que mostra cada ligação carbono-carbono e carbono-hidrogênio.
(CH3)3CCH2CH2CH2C(CH3)2CH2CH(CH2CH3)CH2CH3
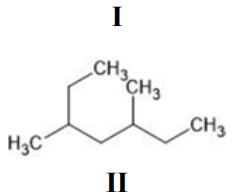
Considerando as informações apresentadas, assinale a opção que mostra a cadeia carbônica na forma de traços correspondente a I.
Provas
A transformação de amônia em nitrogênio molecular pode ocorrer durante o tratamento de água com cloro molecular, conforme equação química a seguir.
2 NH3 (g) + 3 Cl2 (g) → N2 (g) + 6 HCl (g)
Considerando que essa reação foi estudada em um reator fechado e com todos os reagentes em fase gasosa, é correto afirmar que
Provas
A decomposição de O3 é uma reação espontânea que é acelerada pela ação do radical cloro (Cl•) de acordo com as equações químicas descritas a seguir.
\(\begin{array}{rcl} Cl^{\cdot} + O_3 & \rightarrow & ^{\cdot}ClO + O_2 \\ ^{\cdot}ClO + ^{\cdot}O & \rightarrow & ^{\cdot}Cl + O_2 \\ \hline O_3 + O & \rightarrow & 2O_2 \end{array}\)
Como base nessas informações, assinale a opção em que é apresentado o gráfico de variação de energia livre em função da coordenada de reação que representa corretamente a decomposição de O3 acelerada por Cl•.
Provas
Para estudar os aspectos cinéticos da reação entre o ozônio (O3) e uma substância orgânica solúvel em água (S), um grupo de técnicos químicos realizou experimentos que mediram o impacto da variação da concentração de O3 e de S na velocidade dessa reação, a partir da equação química a seguir.
S + O3 → S-O3 → produtos de oxidação de S
Os resultados desse estudo estão apresentados nos gráficos a seguir.
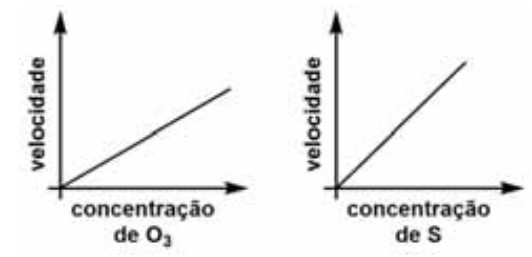
A partir das informações fornecidas nessa situação hipotética, é correto afirmar que a reação estudada pode ser descrita pela lei de velocidade
Provas
O dióxido de carbono e trióxido de enxofre são importantes gases encontrados na atmosfera que reagem com vapor d’água de acordo com as equações químicas a seguir.
CO2 + H2O → H2CO3
SO3 + H2O → H2SO4
Com base nessas informações, é possível afirmar que CO2 e SO3 são óxidos
Provas
A água (H2O) e o isoctano (2,2,4-trimetilpentano), um importante componente da gasolina, apresentam uma significativa diferença entre suas massas molares, mas têm virtualmente a mesma temperatura de ebulição. Isso pode ser explicado porque as forças intermoleculares mais importantes para garantir que amostras puras de água e isoctano sejam líquidas à 25 °C e 1 atm são, respectivamente,
Provas
| Ligação | Energia de Ligação (kJ.mol-1) |
|---|---|
| C-H | 413 |
| O=O | 498 |
| C=O | 803 |
| O-H | 462 |
O metano (CH4) é um gás gerado pela decomposição anaeróbica de matéria orgânica. Ele entra em decomposição espontânea na presença de oxigênio molecular (O2) e forma gás carbônico (CO2) e água (H2O).
Com base nessas informações e nas entalpias de ligação apresentadas na tabela precedente, é correto afirmar que essa transformação
Provas
Caderno Container