Foram encontradas 36.167 questões.
Um dispositivo eletrônico contém um tubo selado com
gás neônio puro, que, a 27 ºC, apresenta a pressão igual
a 1,2 atm. Considerando que, nesse tubo, o gás neônio
se comporta como gás ideal e que a constante dos gases
é R = 0,08 atm.L.mol–1
.K–1, a densidade do gás neônio no
tubo é de aproximadamente
Provas
Questão presente nas seguintes provas
A piridina (C5
H5
N) é um reagente versátil usado em solução aquosa em alguns procedimentos analíticos. A equação da reação de hidrólise da piridina é representada na
equação:
C5 H5 N (l) + H2O (l) → C5 H6 N+ (aq) + OH– (aq) K = 2 x 10–9
Uma solução preparada em um balão volumétrico de 100 mL empregou água destilada e 0,005 mol de piridina. O pH dessa solução é igual a
C5 H5 N (l) + H2O (l) → C5 H6 N+ (aq) + OH– (aq) K = 2 x 10–9
Uma solução preparada em um balão volumétrico de 100 mL empregou água destilada e 0,005 mol de piridina. O pH dessa solução é igual a
Provas
Questão presente nas seguintes provas
Considere as equações de reação a seguir, que apresentam a amônia como reagente:
1 – AgCl (s) + 2 NH3 (aq) → [Ag(NH3) 2 ]Cl aq)
2 – NH3 (g) + HI (g) → NH4 I (s)
3 – NH3 + CH3– → CH4 + NH2– ; essa reação ocorre em meio de amônia líquida.
De a cordo com a teoria ácido-base de Lewis, na reação 1, a amônia é classificada como .
De acordo com a teoria ácido-base de Brosted-Lowry, a amônia é classificada, na reação 2, como e, na reação 3, como .
Assinale a alternativa que preenche, correta e respectivamente, as lacunas do texto.
1 – AgCl (s) + 2 NH3 (aq) → [Ag(NH3) 2 ]Cl aq)
2 – NH3 (g) + HI (g) → NH4 I (s)
3 – NH3 + CH3– → CH4 + NH2– ; essa reação ocorre em meio de amônia líquida.
De a cordo com a teoria ácido-base de Lewis, na reação 1, a amônia é classificada como .
De acordo com a teoria ácido-base de Brosted-Lowry, a amônia é classificada, na reação 2, como e, na reação 3, como .
Assinale a alternativa que preenche, correta e respectivamente, as lacunas do texto.
Provas
Questão presente nas seguintes provas
Dentre diversos compostos binários, o composto que, ao
interagir com água destilada, se comporta como ácido de
Ahrrenius é aquele constituído por hidrogênio e
Provas
Questão presente nas seguintes provas
O resultado do estudo da cinética da decomposição de
um certo princípio ativo de um medicamento revelou que
a sua decomposição obedece ao mecanismo cinético de
primeira ordem e que, quando exposto continuamente a
40 ºC, em 12 meses, esse princípio ativo degrada 75%
de sua quantidade inicial no medicamento.
A meia vida desse princípio ativo exposto continuamente
a 40 ºC é:
A meia vida desse princípio ativo exposto continuamente a 40 ºC é:
A meia vida desse princípio ativo exposto continuamente a 40 ºC é:
Provas
Questão presente nas seguintes provas
Um professor apresentou os seguintes potenciais-padrão
de redução para que seus alunos propusessem uma pilha a partir deles.
Ni2+ (aq) + 2e– → Ni (s) Eº = – 0,23 V
Mn2+ (aq) + 2e– → Mn (s) Eº = – 1,18 V
O metal que os alunos devem escolher como catodo e o valor do potencial-padrão (ddp) teórico dessa pilha, respectivamente, são:
Ni2+ (aq) + 2e– → Ni (s) Eº = – 0,23 V
Mn2+ (aq) + 2e– → Mn (s) Eº = – 1,18 V
O metal que os alunos devem escolher como catodo e o valor do potencial-padrão (ddp) teórico dessa pilha, respectivamente, são:
Provas
Questão presente nas seguintes provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias Inorgânicas
Leia o texto a seguir para responder à questão:
No Brasil, o uso de aditivos químicos nos alimentos obedece
a regulamentações do Ministério da Saúde e ocorre por razões sanitárias, tecnológicas ou sensoriais. Uma classe de
antimicrobianos utilizada são sais dos ânions sulfito (SO32–) e
hidrogenossulfito (HSO3–
), além do dióxido de enxofre (SO2).
O controle de qualidade para monitorar os teores dessas espécies químicas nos produtos alimentícios é feito em várias
etapas do processo de produção por meio de análises químicas. Uma dessas análises emprega a reação representada
na equação a seguir:
HSO3–
(aq) + I2
(s) + H2O (l) → SO4
2–
(aq) + 3H+ (aq) + 2I–
(aq)
Os limites máximos de compostos de enxofre nos alimentos
são expressos na forma de SO2
residual. Nos vinhos, os teores máximos de dióxido de enxofre residual devem ser de
0,032g em 100 mL da bebida.
Provas
Questão presente nas seguintes provas
Leia o texto a seguir para responder à questão:
No Brasil, o uso de aditivos químicos nos alimentos obedece
a regulamentações do Ministério da Saúde e ocorre por razões sanitárias, tecnológicas ou sensoriais. Uma classe de
antimicrobianos utilizada são sais dos ânions sulfito (SO32–) e
hidrogenossulfito (HSO3–
), além do dióxido de enxofre (SO2).
O controle de qualidade para monitorar os teores dessas espécies químicas nos produtos alimentícios é feito em várias
etapas do processo de produção por meio de análises químicas. Uma dessas análises emprega a reação representada
na equação a seguir:
HSO3–
(aq) + I2
(s) + H2O (l) → SO4
2–
(aq) + 3H+ (aq) + 2I–
(aq)
Os limites máximos de compostos de enxofre nos alimentos
são expressos na forma de SO2
residual. Nos vinhos, os teores máximos de dióxido de enxofre residual devem ser de
0,032g em 100 mL da bebida.
Provas
Questão presente nas seguintes provas
Dois cilindros mantidos sob a mesma temperatura contêm gases puros, oxigênio (O2) no cilindro 1 e ozônio (O3) no cilindro 2. O volume do gás O3 é equivalente a 1/2 do volume do gás O2 . Os dois gases estão sob a mesma pressão.
Considerando que a massa molar do O2 é 32 g/mol e que a massa molar do O3 é 48 g/mol, a relação
\(\frac{\text{massa do gás do cilindro 1 } (m_{O_{2}})}{\text{massa do gás do cilindro 2 } (m_{O_{3}})}\)
é igual a
Provas
Questão presente nas seguintes provas
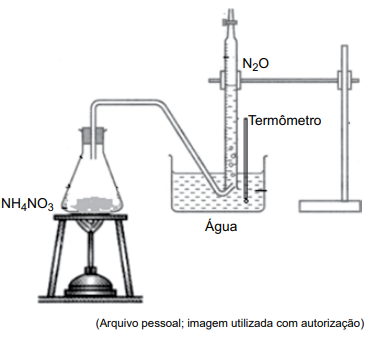
Leia o texto e analise a figura a seguir para responder à questão:
Na figura, é apresentado o esquema da aparelhagem empregada em um experimento de química.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container