Foram encontradas 36.278 questões.
O elemento químico de menor número atômico é o mais abundante no Universo. Ele possui quantidade de prótons igual a 1 e faz parte da composição da água. Esse elemento químico é denominado:
Provas
Para a produção de uma solução antisséptica à base de iodo, foram empregados 0,02 mol de I2, 0,06 mol de KI e determinada quantidade de água.
A massa total de iodo, em gramas, presente nessa solução é igual a:
Provas
Para aumentar a eficiência energética de uma caldeira industrial, pesquisadores realizaram um teste que verificou a expansão volumétrica de uma amostra de gás ideal em função da temperatura. Observe os resultados no gráfico:
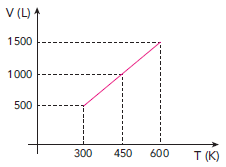
Admita que o processo de expansão volumétrica ocorre à pressão constante de 8 atm e que a constante universal dos gases ideais é de 0,08 atm.L/mol.K.
Ao atingir a temperatura máxima, o número de mols da amostra de gás corresponderá a:
Provas
Em um dispositivo, é inserida uma mistura heterogênea de água e óleo. A mistura passa por um processo de separação e, com o auxílio de uma torneira, regula-se a saída do líquido de maior densidade, conforme ilustrado abaixo.
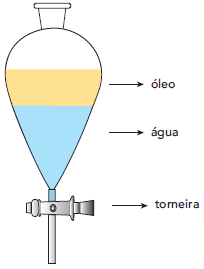
Tal processo de separação é denominado:
Provas
Observe a equação química que representa a hidrólise do carbeto de cálcio.
\( CaC_2(s)+2\, H_2O(\ell) \rightarrow Ca(OH)_2(aq)+C_2H_2(g) \)
O nome do composto orgânico obtido nessa reação é:
Provas
Ao anoitecer, as células da retina envolvidas na percepção da luminosidade disparam sinais que estimulam a glândula pineal a produzir e secretar melatonina, hormônio responsável por preparar o organismo para o repouso. Por ser composta por uma porção hidrofílica e outra hidrofóbica, a melatonina penetra facilmente a membrana plasmática de diferentes tipos de células.
Essa facilidade de penetração da melatonina deve-se à composição da membrana plasmática, que contém moléculas dos seguintes tipos:
Provas
Dentre os elementos químicos do quinto período da tabela de classificação periódica, sabe-se que apenas o xenônio é encontrado no estado gasoso sob condições ambientes. Isso se explica pela alta estabilidade desse elemento, o que resulta em fracas interações interatômicas.
A característica do xenônio que justifica essa estabilidade é:
Provas
COM BASE NO TEXTO A SEGUIR, RESPONDA A QUESTÃO.
Os chamados radicais livres, que resultam de reações de oxidação no interior das células eucariontes, podem produzir mutações gênicas, contribuindo, por exemplo, para o envelhecimento dos tecidos ao longo do tempo. Esses radicais são degradados pela enzima superóxido dismutase, processo que gera uma substância tóxica. Essa substância, por sua vez, é decomposta pela catalase no interior de uma estrutura celular específica.
O ânion superóxido é uma espécie química oxidante que possui dois átomos de oxigênio e carga -1, sendo capaz de formar compostos binários com metais alcalinos e alcalino-terrosos. Sabendo que o cálcio é um metal alcalino-terroso, a fórmula química do superóxido de cálcio corresponde a:
Provas
O fósforo branco, quando em contato com o oxigênio, entra em combustão espontânea, causando graves consequências se usado em armamentos. Observe a equação da reação química entre essas duas substâncias:
P4 (s) + 5 O2 (g) → P4O10 (s)
Na reação de 248 g de P4, a massa de O2 consumida, em gramas, corresponde a:
Provas
Em análises químicas, a presença de bases inorgânicas em uma amostra é identificada com o emprego de substâncias que adquirem cor ao reagir com o ânion dessas bases.
A fórmula desse ânion é:
Provas
Caderno Container