Foram encontradas 36.273 questões.
TABELA PERIÓDICA
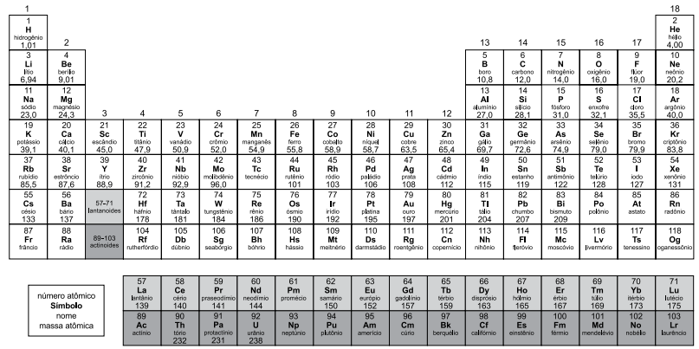
Notas: Os valores de massas atômicas estão apresentados com três algarismos significativos. Não foram atribuídos valores às massas atômicas de elementos artificiais ou que tenham abundância pouco significativa na natureza. Informações adaptadas da tabela IUPAC 2016.
A reação representada pela equação a seguir ocorre em uma única etapa estabelecendo-se equilíbrio entre reagente (R) e produto (P).
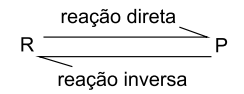
A energia da reação direta é igual a – 100kJ/mol e a energia de ativação da reação direta é igual a 140 kJ/mol. Com a adição de um catalisador, a energia de ativação da reação direta diminui 60 kJ/mol, fazendo com que a energia de ativação da reação inversa seja igual a
Provas
TABELA PERIÓDICA

Notas: Os valores de massas atômicas estão apresentados com três algarismos significativos. Não foram atribuídos valores às massas atômicas de elementos artificiais ou que tenham abundância pouco significativa na natureza. Informações adaptadas da tabela IUPAC 2016.
O composto H3BO3 (massa molar = 61,6 g/mol) é um sólido branco cristalino que, ao ser solubilizado em água, forma o ácido bórico, um ácido monoprótico, que em dada temperatura apresenta Ka = 5 x 10–10. Nessa condição de temperatura, usando-se um balão volumétrico de 100 mL e água destilada para se preparar uma solução de ácido bórico com pH = 5,0, a massa de H3BO3 que deve ser pesada é igual a
Provas
TABELA PERIÓDICA

Notas: Os valores de massas atômicas estão apresentados com três algarismos significativos. Não foram atribuídos valores às massas atômicas de elementos artificiais ou que tenham abundância pouco significativa na natureza. Informações adaptadas da tabela IUPAC 2016.
Uma amostra contendo 100 mg de uma mistura de carbonato de cálcio e de óxido de cálcio foi analisada por termogravimetria com aquecimento até 800 ºC em atmosfera de ar. A termogravimetria é uma técnica analítica em que a amostra é aquecida em um forno acoplado a uma balança e a massa da amostra é medida durante o aquecimento. Ao término da análise, o resíduo final apresentou a massa constante de 89 mg.
O teor de carbonato de cálcio na amostra analisada corresponde a:
Provas
TABELA PERIÓDICA

Notas: Os valores de massas atômicas estão apresentados com três algarismos significativos. Não foram atribuídos valores às massas atômicas de elementos artificiais ou que tenham abundância pouco significativa na natureza. Informações adaptadas da tabela IUPAC 2016.
Um certo metal, M, forma o óxido estável de fórmula unitária MO2 . O cátion Mx+ presente nesse óxido tem configuração eletrônica
Mx+= [Ar] 3d1
O metal M é o elemento
Provas
I. O DNA é formado por duas cadeias de polinucleotídeos (fita), que são constituídas por vários nucleotídeos. Os nucleotídeos são unidos uns aos outros por ligações denominadas fosfodiéster.
II. Sequências de DNA formam os cromossomos.
III. Cada organismo tem um número semelhante de cromossomos. O ser humano, por exemplo, tem 46 (recebemos 23 da mãe e outros 23 do pai).
IV. Em todos os seres vivos, o DNA é formado por uma fita dupla composta por uracila, timina, citosina e guanina.
Provas
I. A vitamina C também pode ser chamada de ácido ascórbico.
II. O ácido ascórbico é considerado uma substância cristalina e de cor branca, solúvel em água e álcool que está classificada no grupo de vitaminas lipossolúveis, pois possuem facilidade de absorção, circulam pelo sistema e são excretadas pela urina.
III. Sabe-se que o ácido ascórbico em solução aquosa é facilmente oxidado, tornando-o um ótimo oxidante protegendo outras espécies químicas de se oxidarem. Deste modo um exemplo da ação do ácido ascórbico, é visivelmente reparado quando corta-se uma fruta, tal como uma maçã que, em questão de pouco tempo a mesma escurece; isso acontece porque compostos fenólicos naturais oxidam na presença de enzimas e do oxigênio presente no ar. Quando esses compostos das frutas oxidam, eles geram as quinonas, que podem sofrer polimerização e formar pigmentos escuros e insolúveis.
Marque a alternativa correta, considerando a análise das proposições:
Provas
I. 6 CO2 +12 H2O → C6H12O6 + 6 O2 + 6 H2O
II. C6H12O6 + 6O2 → 6CO2 + 6H2O + energia
Marque a alternativa correta.
Provas
Concentração de Fosfato (μmol.L – 1 ) Absorbância (A) 5,00 0,08 10,0 0,16 20,0 0,33 40,0 0,65 50,0 0,81
Uma determinada amostra, ao ser analisada, apresentou absorbância de 0,57. Utilizando os dados da curva de calibração acima, a concentração de fosfato encontrada é:
Provas
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Dado: Ka (HA) = 2,5.10 − 4 mol.L− 1
Provas
Caderno Container