Foram encontradas 36.242 questões.
O esquema mostra a pilha formada por eletrodos de níquel e cobre. O quadro da sequência traz os potenciais-padrão de redução desses eletrodos.
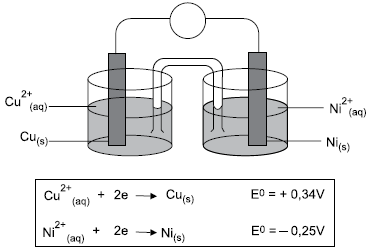
Considerando a constante de Faraday igual a 9,65 × 104 C.mol–1, a energia livre de Gibbs para essa pilha é
Provas
O esquema a seguir representa o funcionamento de uma bateria do tipo íon lítio, cuja equação global é representada pela equação:
LixCoO2 (s) + LiyC6 (s) → Lix+yCoO2 (s) + C6 (s).
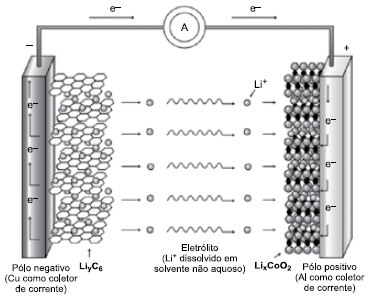
De acordo com o esquema, durante a descarga da bateria
Provas
Considere o diagrama de fases para a substância hidrazina, usada em propelentes de foguetes.
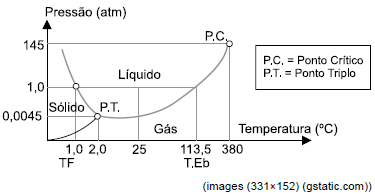
Na temperatura de 390 ºC, a hidrazina é um
Provas
Considere os compostos orgânicos:
I. ETÓXI-METANO
II. PENTANOL
III. ÁCIDO METANOICO
IV. ETANAL
V. PENT-2-ONA
Estabelecem ligações intermoleculares do tipo ligação de hidrogênio e possuem a maior solubilidade em água, respectivamente, os compostos:
Provas
As geometrias das moléculas dos compostos C!$ \ell !$O2, PC!$ \ell !$5, SF6 e SF4 são, respectivamente:
Provas
A ordem crescente para a primeira energia de ionização dos elementos C, Ge, Ca e Sr é:
Provas
O elemento químico estrôncio, Sr, possui quatro isótopos naturais: 84Sr, 86Sr, 87Sr e 88Sr. Sabendo que as porcentagens isotópicas menores são 84Sr = 0,56%, 86Sr = 9,86%, 87Sr = 7,02% e a massa atômica desse elemento é 87,62 u, a massa relativa ao 88Sr na composição da massa atômica e sua porcentagem natural são, respectivamente,
Provas
A mistura entre íons permanganato e peróxido, em meio ácido, pode ser representada pela seguinte equação não balanceada:
MnO4 –(aq) + H2O2(aq) + H+(aq) → Mn2+(aq) + O2(g) + H2O(!$ \ell !$)
Considerando as semirreações e seus potenciais de redução, a 25 ºC,
O2 + 2 H+ + 2 e– → H2O2; E0 = + 0,68 V
MnO4 –(aq) + 8 H+(aq) + 5 e– → Mn2+(aq) + 4 H2O(!$ \ell !$); E0 = +1,51 V
conclui-se que o potencial da reação global e os coeficientes estequiométricos menores e inteiros que completam a equação são:
Provas
No mecanismo que mostra a reação de desidratação de um álcool, os asteriscos nos intermediários 1 e 2 indicam ligações incompletas dos respectivos átomos de carbono.
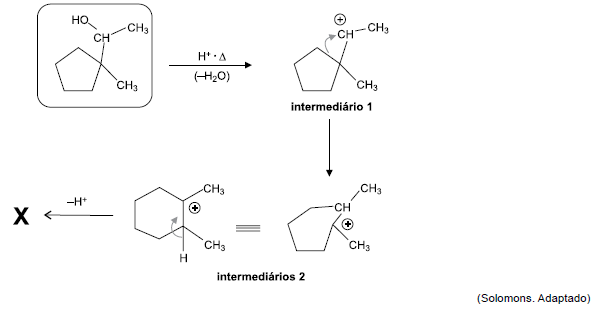
A estrutura de X que representa o produto principal da reação é:
Provas
A 100 mL de uma solução contendo 1×10–2 mol.L–1 em íons Mg2+ foram adicionados 100 mL de hidróxido de sódio 0,10 mol.L–1 precipitando Mg(OH)2 (kps, a 25 ºC = 9×10–12). A concentração de íons Mg2+ em solução, após a reação é de
Provas
Caderno Container