Foram encontradas 36.174 questões.
Os compostos hidroxiacetona (1-hidroxi-propan-2-ona), etanoato
de metila e ácido propanoico foram recentemente identificados
no espaço interestelar. Eles estão inseridos numa classe
denominada “compostos orgânicos complexos” e suas rotas de
síntese nesse meio despertam grande interesse científico.
Dedica-se grande esforço também à compreensão do papel
exercido por tais compostos orgânicos complexos na síntese
abiótica de biomoléculas também encontradas nas mesmas
regiões.
A esse respeito, assinale V para a afirmativa verdadeira e F para a falsa.
( ) Hidroxiacetona, etanoato de metila e ácido propanoico são isômeros. ( ) Hidroxiacetona, etanoato de metila e ácido propanoico apresentam grupos polares em suas estruturas. ( ) Pontos de ebulição dos compostos seguem a ordem: etanoato de metila > ácido propanoico ≈ hidroxiacetona.
As afirmativas são, respectivamente,
A esse respeito, assinale V para a afirmativa verdadeira e F para a falsa.
( ) Hidroxiacetona, etanoato de metila e ácido propanoico são isômeros. ( ) Hidroxiacetona, etanoato de metila e ácido propanoico apresentam grupos polares em suas estruturas. ( ) Pontos de ebulição dos compostos seguem a ordem: etanoato de metila > ácido propanoico ≈ hidroxiacetona.
As afirmativas são, respectivamente,
Provas
Questão presente nas seguintes provas
Diborano (B2H6) é um gás incolor com odor repulsivamente doce.Mistura-se facilmente com o ar formando uma mistura explosiva,pois sofre ignição espontaneamente em ar úmido à temperaturaambiente.
Considere os dados termoquímicos:
B2H6(g) + 3 O2(g) → B2O3(s) + 3 H2O(g) ΔHº= -1941 kJ mol–1 2 B(s) + 3/2 O2(g) → B2O3(s) ΔHº= -2368 kJ mol–1 H2(g) + 1/2 O2(g) → H2O(g) ΔHº= -241,8 kJ mol–1
A entalpia padrão de formação do diborano (em kJ mol–1) é
Considere os dados termoquímicos:
B2H6(g) + 3 O2(g) → B2O3(s) + 3 H2O(g) ΔHº= -1941 kJ mol–1 2 B(s) + 3/2 O2(g) → B2O3(s) ΔHº= -2368 kJ mol–1 H2(g) + 1/2 O2(g) → H2O(g) ΔHº= -241,8 kJ mol–1
A entalpia padrão de formação do diborano (em kJ mol–1) é
Provas
Questão presente nas seguintes provas
Deseja-se construir um sistema eletroquímico contendo um
catodo de cobre (no qual o metal estará imerso em uma solução
aquosa de nitrato de cobre) e um anodo de alumínio (no qual o
metal estará imerso em solução aquosa de sulfato de alumínio).
Os dois eletrodos estarão conectados por uma ponte salina,
contendo solução aquosa de nitrato de potássio e, externamente,
por um fio de cobre condutor.
[Dados. Potenciais de redução padrão:
E0Al3+|Al = -1,66 V; E0Cu2+|Cu = +0,34 V.]
Nessas condições, analise as afirmativas a seguir a respeito desse sistema eletroquímico:
I. Será uma pilha, pois a reação esperada é espontânea. II. A diferença de potencial esperada é 7,32V. III. Será uma reação espontânea se um potencial externo de 2,00V for aplicado ao sistema.
Está correto o que se afirma em
[Dados. Potenciais de redução padrão:
E0Al3+|Al = -1,66 V; E0Cu2+|Cu = +0,34 V.]
Nessas condições, analise as afirmativas a seguir a respeito desse sistema eletroquímico:
I. Será uma pilha, pois a reação esperada é espontânea. II. A diferença de potencial esperada é 7,32V. III. Será uma reação espontânea se um potencial externo de 2,00V for aplicado ao sistema.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
Dois recipientes contêm metano e amônia, respectivamente,
ambos com volume de 10L, e estão sob mesma temperatura
(425K) e pressão (0,85 bar).
[Dados: massas molares (em g.mol-1). Metano: 16; Amônia: 17.]
Nesse caso, é correto afirmar que os recipientes contêm
[Dados: massas molares (em g.mol-1). Metano: 16; Amônia: 17.]
Nesse caso, é correto afirmar que os recipientes contêm
Provas
Questão presente nas seguintes provas
A análise elementar tem por objetivo identificar e quantificar
elementos químicos como carbono, hidrogênio, nitrogênio e
enxofre com excelente precisão em compostos presentes em
amostras puras líquidas ou sólidas. Os resultados da análise
elementar permitem identificar a fórmula mínima do composto
químico.
A análise elementar de uma amostra revelou a seguinte composição: 58,5% de carbono, 4,1% de hidrogênio e 11,4 % de nitrogênio.
[Dados: massas molares (em g.mol-1): C: 12; H: 1; N: 14; O: 16.]
A fórmula mínima do composto na amostra é
A análise elementar de uma amostra revelou a seguinte composição: 58,5% de carbono, 4,1% de hidrogênio e 11,4 % de nitrogênio.
[Dados: massas molares (em g.mol-1): C: 12; H: 1; N: 14; O: 16.]
A fórmula mínima do composto na amostra é
Provas
Questão presente nas seguintes provas
Durante uma aula sobre transformações dos materiais, os alunos
realizaram a seguinte atividade: colocaram um pouco de vinagre
em uma garrafa e prenderam um balão contendo bicarbonato de
sódio no gargalo; em seguida, deixaram o bicarbonato cair sobre
o vinagre e observaram a mistura borbulhar e o balão encher.
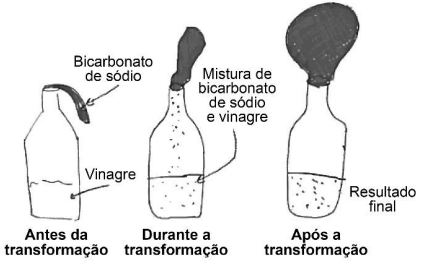
Após compararem as características das substâncias usadas no experimento, antes e depois da transformação, os alunos concluíram, corretamente, que ocorreu um fenômeno

Após compararem as características das substâncias usadas no experimento, antes e depois da transformação, os alunos concluíram, corretamente, que ocorreu um fenômeno
Provas
Questão presente nas seguintes provas
Sabendo que o elemento químico Prata apresenta número atômico 47, a representação do nível
eletrônico ocupado mais externo (nível de valência) para este átomo (neutro) está corretamente
apresentado em:
Provas
Questão presente nas seguintes provas
Alotropia é o fenômeno que ocorre quando um elemento químico forma duas ou mais substâncias
simples diferentes. Acerca do tema, assinale a alternativa que apresenta uma substância considerada
forma alotrópica do grafite.
Provas
Questão presente nas seguintes provas
Considere a estrutura química da testosterona.
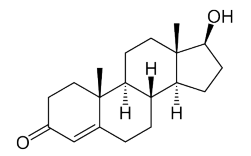
A massa molar para a estrutura química fornecida na imagem será, aproximadamente, de:
Dados de massas molares: C = 12 g/mol, H = 1 g/mol e O = 16 g/mol.
Provas
Questão presente nas seguintes provas
Considere a seguinte reação química, não-balanceada.
C2H6O + O2 → CO2 + H2O
Para a reação descrita, 3,0 g de C2H6O foi adicionado a um ambiente contendo 100,0 g de oxigênio. A massa (g) de CO2 produzida será, aproximadamente, de:
Dados de massas molares: C = 12 g/mol, H = 1 g/mol e O = 16 g/mol.
C2H6O + O2 → CO2 + H2O
Para a reação descrita, 3,0 g de C2H6O foi adicionado a um ambiente contendo 100,0 g de oxigênio. A massa (g) de CO2 produzida será, aproximadamente, de:
Dados de massas molares: C = 12 g/mol, H = 1 g/mol e O = 16 g/mol.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container