Foram encontradas 36.167 questões.
A camada de ozônio funciona naturalmente como um ‘escudo protetor’, ao filtrar o UV-B nocivo aos seres vivos. Os principais gases que destroem a camada de ozônio são os clorofluorcarbonetos e hidrofluorcarbono. NÃO é um elemento químico presente na composição dos gases descritos como agentes destruidores da camada de ozônio:
Provas
Sobre o processo eletrolítico para obtenção de elementos químicos isolados, analise as afirmativas a seguir:
I. A eletrólise é um processo no qual o trabalho elétrico gera a reação química.
II. Se o cloreto de sódio for submetido a uma eletrólise ígnea ou aquosa, os produtos dessa reação são os mesmos: sódio metálico e gás cloro.
III. Na eletrólise em meio aquoso, quem irá definir a ordem de descarga dos íons é o potencial de redução padrão, E°red, de cada substância durante esse processo.
IV. A quantidade formada de produtos eletroquímicos será definida pela primeira lei de Faraday.
É CORRETO o que se afirma em
Provas
A agricultura global, anualmente, demanda cerca de 80 milhões de toneladas de fertilizantes nitrogenados (Biologia e Mudanças Climáticas no Brasil, 2008). A preocupação com a possível escassez desse elemento para suprir as atividades agrárias implicaria uma escassez de alimento, inviabilizando o sustento de bilhões de pessoas. Com o objetivo de minimizar essa escassez o processo de Haber-Bosch, é um procedimento que tem como finalidade a produção de fertilizantes sintéticos por meio da reação do nitrogênio gasoso N2 com o hidrogênio a alta pressão (200 atm) e temperatura (450ºC), gerando como subproduto a amônia (NH3) (M. G., et al. 2003), através da reação química: N2(g) + 3H2(g) → 2 NH3(g) + energia. Considerando a constante dos gases ideais como sendo 0,082 atm.L/mol.K, os volumes em litros para 1 mol de nitrogênio gasoso e para 2 mols de amônia, nas condições termodinâmicas descritas acima são, respectivamente:
Provas
Em 2020, o mundo passou a conviver com a pandemia do coronavírus causador da doença COVID-19. Uma das profilaxias recomendadas pela Organização Mundial da Saúde (OMS), além do uso de máscara e do distanciamento social, foi a higienização e assepsia com álcool etílico 70° INPM. Contudo, o uso displicente de álcool gel tem causado diversos acidentes domésticos, como queimaduras acidentais. Em situações como essa, a equação química balanceada que corresponde à queima de álcool gel é
Provas
Considere o preparo de 50 mL de uma solução de nitrato de prata 0,092 mol L-1. Após a sua diluição em água em um balão volumétrico, a concentração final dessa solução NÃO está correta porque a
Provas
Considere as seguintes descrições de um composto orgânico A:
1 – Apresenta 5 (cinco) átomos de carbono em sua cadeia carbônica, classificada como aberta, ramificada e insaturada.
2 – A estrutura da cadeia carbônica apresenta apenas 1 (um) carbono com hibridização do tipo sp, apenas 2 (dois) carbonos com hibridização sp2 e os demais carbonos com hibridização sp3.
3 – O composto é um alcadieno com massa molar de 68,0 g mol-1.
Dados:
| Ligação |
Energia de ligação (kJ mol-1; 25 ºC e 1 atm) |
Ligação | Energia de ligação (kJ mol-1; 25 ºC e 1 atm) |
| C – C |
348 | O = O |
495 |
| C = C |
614 |
C = O |
799 |
| H – O |
463 |
C – H |
413 |
| volume molar gasoso nas Condições Normais de Temperatura e Pressão (CNTP) = 22,4 L mol-1 |
|||
Em relação ao composto acima descrito são feitas as seguintes afirmativas:
I – Considerando as características descritas do composto A, a nomenclatura regulada pela União Internacional de Química Pura e Aplicada (IUPAC) é 3-metilbut-1,2-dieno.
II – O volume liberado, nas Condições Normais de Temperatura e Pressão, a partir de 20,4 g do composto A, é de 6,72 L de CO2, considerando a combustão completa, rendimento de 100% e comportamento de gás ideal.
III – O composto A é completamente solúvel em água.
IV – A entalpia de combustão teórica do composto A é de 3001 kJ mol-1.
V – O composto A apresenta em sua estrutura apenas 1 (um) carbono secundário.
Das afirmativas feitas, estão corretas apenas
Provas
A elaboração de representações científicas é muito importante para organizar observações e conclusões resultantes do trabalho de pesquisa dos cientistas. Na Química, um dos mais emblemáticos exemplos dessa prática são os modelos atômicos. Cada um reúne a contribuição de diversos estudiosos, apesar de geralmente ser atribuído a apenas um deles. Nas alternativas abaixo, são apresentados alguns dos modelos atômicos (por meio da referência nominal aos seus respectivos elaboradores) e os nomes de alguns cientistas cujos trabalhos, citados entre parênteses, contribuíram para a elaboração de alguns desses modelos. Podemos afirmar que a relação entre o modelo atômico e o estudioso cujo trabalho contribuiu para a construção do respectivo modelo está corretamente apresentada na alternativa:
Provas
As recentes tensões militares no leste europeu reacenderam preocupações mundiais sobre um local sensível: a Usina Nuclear de Chernobyl. Na madrugada do dia 26 de abril de 1986, em decorrência de falhas estruturais e humanas, um dos reatores da Usina explodiu, expondo parte do seu material radioativo. Um dos isótopos radioativos presentes na Usina no momento do acidente era o Césio-137, cuja meia-vida é de aproximadamente 30 anos.
Dado: \( \sqrt[5] {2} \) = 1,15
Baseado nestas informações, são feitas as seguintes afirmativas:
I – O porcentual de Césio-137 que permanecia na Usina no dia 26 de abril de 2022, em relação à quantidade presente no momento da explosão, desconsiderando quaisquer perdas de material não relacionadas ao decaimento radioativo, era de aproximadamente 43%.
II – O decaimento de um átomo de \( 137 \\ 55 \)Cs formando um átomo de \( 137 \\ 56 \)Ba evidencia a emissão de uma partícula alfa (\( \alpha \)).
III – Quando uma partícula beta (\( \beta \)) é emitida, o número atômico (Z) aumenta em uma unidade, pois surge um novo próton da decomposição de um nêutron presente no núcleo, porém o número de massa (A) não se altera.
IV – a radiação gama emitida por um átomo de \( 137 \\ 55 \)Cs permanece no organismo humano por um período de meia-vida semelhante ao do radioisótopo.
Das afirmativas feitas, estão corretas apenas
Provas
Em relação à equação não balanceada a seguir, que representa o processo de obtenção de ferro a partir do óxido de ferro III presente no minério hematita, são feitas as seguintes afirmações:
Fe2O3 (s) + C (s) → Fe (s) + CO (g)
Dados: volume molar gasoso nas Condições Normais de Temperatura e Pressão (CNTP) = 22,4 L mol-1 constante de Avogadro = 6,0 x 1023 mol-1
I – A partir de 25 mol de óxido de ferro III e 960,0 g de carbono, podem ser obtidos 4,50 x 1025 moléculas de monóxido de carbono, considerando-se rendimento de 100% na reação.
II – O estabelecimento da ligação química entre um átomo de ferro e um átomo de oxigênio, no óxido de ferro III, ocorre através de uma ligação covalente polar.
III – A partir de 200,0 kg de hematita com 80% de pureza em relação ao óxido de ferro III, e quantidade suficiente de carbono, podem ser obtidos 67200 L de monóxido de carbono nas CNTP, considerando-se rendimento de 100% na reação.
IV – O monóxido de carbono apresenta geometria linear e é classificado como um óxido anfótero.
V – A obtenção de 130 mol de ferro, a partir de 100 mol de óxido de ferro III e quantidade suficiente de carbono, representaria um rendimento da reação de 65%.
Das afirmativas feitas, estão corretas apenas
Provas
Alexander Williamson foi um químico inglês que viveu entre os anos de 1824 a 1904. Williamson desenvolveu uma rota reacional para síntese de éteres a partir de álcoois, cujo mecanismo é o seguinte:
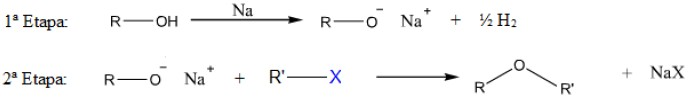
Considere que R e R’ representam radicais hidrocarbonetos e X representa um halogênio. De acordo com a rota reacional apresentada, indique a alternativa que contém a fórmula do éter produzido a partir dos reagentes fenilmetanol e 2-bromo-2-metilpropano.
Provas
Caderno Container