Foram encontradas 36.167 questões.
Sal light é chamado assim porque contém baixo teor de sódio. O tempero com essas características é composto de cloreto de sódio (NaCl) e cloreto de potássio (KCl) e é recomendado para pessoas hipertensas. Uma solução de sal light foi preparada com 100 mL de uma solução de NaCl 0,2 mol/L e 200 mL de uma solução de KCl 2,98 g/L.
Internet: <www.mundoeducacao.uol.com.br> (com adaptações).
A partir do texto apresentado, e considerando que as massas molares do NaCl e do KCl valham, respectivamente, 58,5 g/mol e 74,6 g/mol e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
A solução de sal light é classificada como eletrolítica e a sua condutibilidade elétrica é tão maior quanto menor for a sua concentração.
Provas
Sal light é chamado assim porque contém baixo teor de sódio. O tempero com essas características é composto de cloreto de sódio (NaCl) e cloreto de potássio (KCl) e é recomendado para pessoas hipertensas. Uma solução de sal light foi preparada com 100 mL de uma solução de NaCl 0,2 mol/L e 200 mL de uma solução de KCl 2,98 g/L.
Internet: <www.mundoeducacao.uol.com.br> (com adaptações).
A partir do texto apresentado, e considerando que as massas molares do NaCl e do KCl valham, respectivamente, 58,5 g/mol e 74,6 g/mol e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
A concentração de íons Cl− na solução de sal light preparada conforme o texto é inferior a 0,05 mol/L.
Provas
Sal light é chamado assim porque contém baixo teor de sódio. O tempero com essas características é composto de cloreto de sódio (NaCl) e cloreto de potássio (KCl) e é recomendado para pessoas hipertensas. Uma solução de sal light foi preparada com 100 mL de uma solução de NaCl 0,2 mol/L e 200 mL de uma solução de KCl 2,98 g/L.
Internet: <www.mundoeducacao.uol.com.br> (com adaptações).
A partir do texto apresentado, e considerando que as massas molares do NaCl e do KCl valham, respectivamente, 58,5 g/mol e 74,6 g/mol e que a constante de Avogadro valha 6 × 1023 mol−1, julgue o item a seguir.
Na solução de sal light preparada conforme o texto, estão contidos 1,2 × 1022 íons de Na+.
Provas
Provas
Com base na nomenclatura dos ácidos, relacione a coluna 1 com a coluna 2:
Coluna 1
(1) H2SO4
(2) HNO3
(3) H2SO3
(4) HNO2
Coluna 2
(__)Ácido nítrico.
(__)Ácido sulfuroso.
(__)Ácido nitroso.
(__)Ácido sulfúrico.
Após análise, assinale a alternativa que apresenta a sequência CORRETA.
Provas
Os polímeros são moléculas de cadeia longa que consistem em unidades repetitivas chamadas de monômeros. Eles podem ser naturais ou sintéticos.
Leia o trecho a seguir e preencha corretamente as lacunas.
Os monômeros do eteno podem reagir um com o outro, quebrando a ligação dupla entre os carbonos e unindo-se formando uma longa cadeia polimérica de polietileno. Este é um exemplo de polímero de . O cloreto de polivinila (PVC) é constituído de monômeros em que um átomo de cloro substitui um dos átomos de hidrogênio do eteno. A temperatura de fusão de um polímero de PVC é do que a do polietileno, considerando-se ambos com o mesmo tamanho de cadeia. Alguns polímeros, denominados de , consistem em dois tipos diferentes de monômeros. Por fim, os polímeros que eliminam um átomo ou um pequeno grupo de átomos durante a polimerização são chamados de polímeros de ; um exemplo desse tipo de polímero é o náilon.
A sequência que preenche corretamente as lacunas do texto é
Provas
As transformações físicas e químicas envolvem trocas de energia, principalmente na forma de calor. No dia a dia e na rotina de laboratório é muito importante conhecer e controlar essas trocas de calor.
A respeito dos conceitos envolvidos sobre entalpia, é INCORRETO afirmar que a
Provas
O salitre consiste em um mineral constituído principalmente por nitrato de potássio. Um experimento avaliou o teor de nitrato de potássio em uma amostra de salitre. Para isso, 400 g de salitre foram colocados para reagir com 160 mL de ácido sulfúrico concentrado, formando bissulfato de potássio e ácido nítrico. No final do processo, o ácido sulfúrico foi totalmente consumido.
Dados: densidade do ácido sulfúrico concentrado= 1,8 g/cm3
Massas molares, em g/mol: H= 1; N= 14; O= 16; K= 39; S= 32)
Qual o teor aproximado, em %, do nitrato de potássio na amostra de salitre?
Provas
A reatividade de alguns metais com a água pode ser prevista com base na sua distribuição eletrônica. Em uma aula prática quatro amostras metálicas de elementos químicos distintos W, X, Y e Z foram adicionadas em água, a velocidade das reações foi observada. Na tabela a seguir está a distribuição eletrônica dos elementos utilizados no experimento.
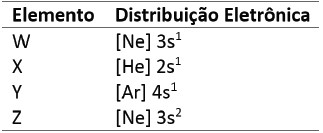
A ordem decrescente de velocidade de reação desses elementos com a água é
Provas
As pilhas consistem em um sistema onde a energia química proveniente de reações redox espontâneas produzem energia elétrica. A pilha de Daniell é um clássico exemplo de célula galvânica que usa a oxidação do cobre pelos íons zinco, conforme a equação representada a seguir:
Zn(s) + Cu2+(aq) !$ → !$ Zn2+(aq) + Cu(s)
| Dado: Zn2+(aq) + 2e-!$ → !$ Znº(s) Eº=-0,76 V Cu2+(aq) + 2e- !$ → !$ Cuº(s) Eº= +0,34 V |
A respeito das células galvânicas em geral e sobre a pilha de Daniell, é correto afirmar que
Provas
Caderno Container