Foram encontradas 35.976 questões.
Sabendo que uma solução de éter etílico — substância utilizada para compor a fase móvel da técnica de separação denominada cromatografia em camada delgada — apresenta ponto de fusão igual a −116,3 ºC e ponto de ebulição igual a 34,6 ºC a uma dada pressão P, julgue os itens a seguir, considerando essa mesma pressão P.
I A −140 ºC o estado do éter etílico é sólido.
II A 23 ºC o estado do éter etílico é gasoso.
III A 34,6 ºC estarão presentes os estados sólido e líquido do éter etílico.
IV A −113 ºC o estado do éter etílico é líquido.
Estão certos apenas os itens
Provas
Um alto explosivo (AE) é um composto cuja detonação é iniciada por calor ou onda de choque, que provoca uma explosão violenta em microssegundos. Um exemplo de AE é o 1,3,5- triamino-2,4,6-trinitrobenzeno (TATB), cuja fórmula é C6H6N6O6. Springall e Robert propuseram um conjunto de regras para predizer os produtos moleculares de uma detonação de explosivos em cuja composição haja carbono, hidrogênio, oxigênio e nitrogênio. A partir dessas regras, é possível descrever os produtos da detonação do composto TATB, de acordo com a equação a seguir.
!$ C_6\,H_6\,N_6\,O_{6(s)} \rightarrow 3 N_{2(g)} + H_2 O_{(g)} + CO_{2(g)} + 3 CO_{(g)} + 2 H_{2(g)} + C_{(s)} !$
Considerando-se essas informações e sabendo-se que M (C6H6N6O6) = 258 g/mol, bem como tendo em vista que, em uma detonação, sejam consumidos 516 g de TATB, é correto concluir que a quantidade de matéria de gases liberados nessa reação será igual a
Provas
Caso 50 mL de uma solução de Mg(OH)2 0,1 mol/L sejam misturados com 50 mL de Mg(OH)2 0,25 mol/L, então, o volume de HCl 5 mol/L necessário para neutralizar completamente 30 mL dessa nova solução básica será
Provas
Para a análise, em laboratório, da presença de certa droga em uma amostra, adquiriu-se 1 mL de um padrão comercial contendo essa droga a uma concentração de 1 mg/mL. No preparo de uma solução estoque para o uso na calibração de um equipamento, um técnico utilizou uma pipeta para transferir 10 μL da solução padrão comercial para um balão volumétrico de 25 mL. Nessa situação hipotética, a concentração final da droga de interesse na solução estoque, em partes por milhão (ppm), seria igual a
Provas
Para o preparo de 250 mL de uma solução de NaCl 0,5 mol/L, sabendo-se que a massa molar do composto é igual a 58,44 g/mol, deve-se dissolver
Provas
Acerca dos fenômenos físicos e químicos, julgue os itens a seguir.
I A formação de ferrugem, após a reação resultante do contato entre ferro e oxigênio, é um fenômeno químico.
II A fundição da prata a 960 ºC é um fenômeno físico.
III A condução de corrente elétrica em um fio de cobre é um fenômeno químico.
Assinale a opção correta.
Provas
O ácido benzoico é muito utilizado na indústria de alimentos para produção de conservantes. A partir do espectro de infravermelho desse ácido, mostrado a seguir, é possível inferir a presença de determinados grupos funcionais e ligações químicas em sua estrutura.
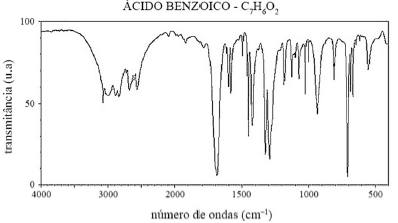
Considerando a imagem e as informações precedentes, assinale a opção correta.
Provas
O cloreto de prata é um sólido branco pouco solúvel em água, porém, quando submetido a aquecimento, pode dissociar-se em íons cloreto e íons prata. Após alguns instantes, os íons em solução atingem o equilíbrio com o sólido. Considerando-se que, quando o equilíbrio for alcançado, a concentração de íons prata seja igual a 1,5 × 10−5 mol/L, é correto afirmar que, nessa condição de equilíbrio, o valor da constante do produto de solubilidade (Kps) para o cloreto de prata é igual a
Provas
Considere que, em um recipiente de 2 L, esteja acontecendo a reação química ilustrada no gráfico a seguir.
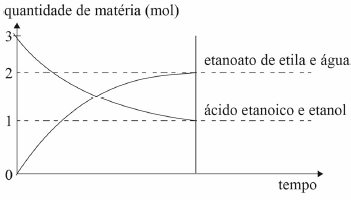
Nesse caso, a constante de equilíbrio da reação em apreço é igual a
Provas
A equação seguinte representa a reação de decomposição da água.
!$ H_2 O(g) \rightleftharpoons H_2(g) + ^1/_2 O_2(g) !$
Considere que, em um recipiente de 5 L, tenham sido adicionados 225 g de água e, em seguida, esse sistema tenha sido aquecido a 2.000 °C, sob pressão de 1 atm. Assumindo-se que, nesse caso, 70% da água será decomposta e que a massa molar da água ( MH2O ) é igual a 18,0 g/mol, é correto afirmar que a concentração de água remanescente, após a situação de equilíbrio, será de
Provas
Caderno Container