Foram encontradas 35.936 questões.
O hidróxido de sódio, sólido bastante higroscópico e reativo com o CO2 do ar, é comumente utilizado na padronização e na dosagem de soluções ácidas em laboratórios. Normalmente, para essas titulações, são utilizadas soluções diluídas de NaOH. Em relação a esse assunto, julgue o item a seguir.
A maneira mais adequada de preparar 100 mL de uma solução de NaOH em determinada concentração em quantidade de matéria é pesar a massa de NaOH necessária e dissolver essa massa em 100 mL de água.
Provas
O hidróxido de sódio, sólido bastante higroscópico e reativo com o CO2 do ar, é comumente utilizado na padronização e na dosagem de soluções ácidas em laboratórios. Normalmente, para essas titulações, são utilizadas soluções diluídas de NaOH. Em relação a esse assunto, julgue o item a seguir.
O NaOH é formado por um metal, um ametal e um gás nobre.
Provas
Considere a sequência reacional e as afirmativas a seguir.
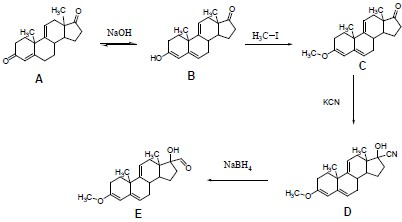
I. A e B são tautômeros.
II. A transformação de B para C é uma reação de adição.
III. Quando D é formado, há a criação de um novo carbono quiral.
IV. A reação de formação de E a partir de D é uma reação de oxidação.
Nesse contexto, é possível afirmar que estão CORRETAS as afirmativas:
Provas
Em relação às estruturas a seguir, assinale a alternativa CORRETA.
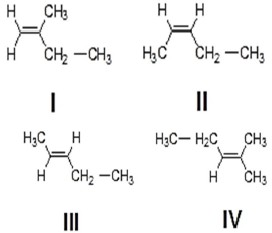
Provas
A atorvastatina é um fármaco utilizado para a redução do colesterol considerado, atualmente, como o fármaco mais vendido de todos os tempos. Apenas nos Estados Unidos, entre os anos de 1992 e 2017, o volume de vendas da atorvastatina foi de cerca de 95 bilhões de dólares.
A seguir é apresentada a estrutura química da atorvastatina.
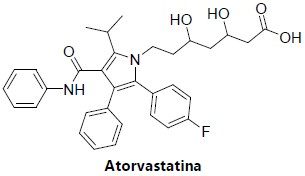
Considere as seguintes afirmativas em relação à estrutura química apresentada:
I. Possui dois carbonos quirais.
II. Possui as funções químicas amida, álcool e haleto orgânico.
III. Possui isomeria geométrica E-Z.
IV. Possui 13 ligações pi.
Nesse contexto, assinale a alternativa CORRETA.
Provas
Foi solicitado a um técnico de laboratório que ele fizesse o descarte de 45 g de um sólido branco cujo rótulo estava ilegível. Ao entrar em contato com a empresa que faria a coleta, ele foi informado de que o material deveria ser fornecido na forma de uma solução aquosa para evitar riscos durante o transporte, e que o preço cobrado para o descarte seria proporcional à massa da solução.
Consultando antigos apontamentos, o técnico verificou que o sólido correspondia a um dos compostos do gráfico a seguir:
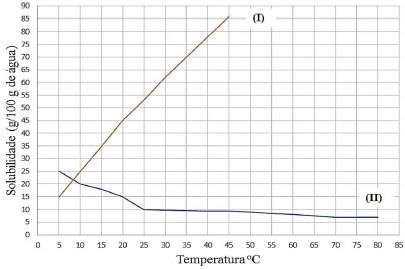
Além disso, ao fazer o teste de solubilidade em água, à temperatura ambiente, foi verificado um aumento da temperatura do sistema após a adição do sólido.
Com base nessas informações, para que o técnico consiga fazer o descarte da maneira mais econômica possível, a massa final da solução preparada, considerando-se que a temperatura do laboratório seja de 20ºC, deve ser:
Provas
Uma promissora alternativa para a produção de energia de maneira mais limpa e sustentável é o uso de hidrogênio no lugar de combustíveis fósseis. No entanto, um dos principais desafios para a implementação desse gás como matriz energética é a sua produção. Atualmente, a maior parte do hidrogênio obtido em escala industrial é preparada através de um processo altamente endotérmico, conhecido como reforma a vapor de metano, que se dá através da reação descrita abaixo:
CH4 (g) + H2O (g) !$ \rightleftharpoons !$ CO (g) + 3 H2 (g)
Considere as seguintes afirmativas em relação ao processo de reforma a vapor de metano:
I. Se adicionarmos água ao sistema, será observado um acréscimo na produção de hidrogênio.
II. Se adicionarmos um catalisador ao sistema, o equilíbrio será deslocado no sentido de favorecer a formação dos produtos.
III. Quando a reação atinge o equilíbrio, a compressão do sistema favorece a reação inversa, levando à produção de metano.
IV. A realização dessa reação em baixa temperatura favorece a produção de hidrogênio.
Nesse contexto, é possível afirmar que estão CORRETAS apenas as seguintes afirmativas:
Provas
Um dos principais métodos utilizados para a contenção da disseminação da COVID-19 é a desinfecção das mãos através do uso de sanitizantes, como o álcool em gel 70% ou o álcool glicerinado 80%. Em um protocolo disponibilizado pela Organização Mundial de Saúde para o preparo de álcool glicerinado 80% estão descritas as seguintes etapas:
I. O etanol é derramado no grande frasco ou tanque até a marca graduada.
II. O peróxido de hidrogênio é adicionado usando o cilindro de medição.
III. O glicerol é adicionado usando um cilindro de medição. Como o glicerol é muito viscoso e adere à parede do cilindro de medição, o cilindro deve ser lavado com água fervida estéril ou destilada e depois esvaziado no frasco / tanque.
IV. O frasco / tanque é então completado até a marca de 10 litros com água destilada estéril ou fervida fria.
V. A tampa ou a tampa de rosca é colocada no tanque / garrafa o mais rápido possível após a preparação, a fim de evitar a evaporação.
VI. A solução é misturada agitando suavemente quando apropriado ou usando uma pá.
Em relação a esse protocolo, assinale a alternativa CORRETA:
Provas
Um dos principais problemas relacionados à extração de petróleo é o entupimento dos poços, que pode ser ocasionado pela precipitação de diferentes sólidos como parafinas, hidratos e carbonatos, dentre eles o carbonato de cálcio. Uma das soluções para esse problema é o emprego de inibidores de precipitação, substâncias que minimizam a formação desses sólidos aumentando o tempo de vida útil do poço.
Com o intuito de estudar a eficiência de um novo inibidor, um grupo de pesquisa realizou um experimento onde foram adicionados em um recipiente: 31,8 g de carbonato de sódio, 200 ml de água, 100 ml de uma solução contendo o inibidor e 200 ml de uma solução 2,5 M de cloreto de cálcio. A mistura permaneceu sob agitação por 30 min e, após esse tempo, verificou-se que o carbonato de cálcio foi formado com um rendimento molar de apenas 5%, atestando a eficiência do inibidor. Com base nessas informações, a massa de carbonato de cálcio obtida foi:
Provas
Nos últimos anos, muito se falou sobre o potencial estratégico do Brasil como fornecedor mundial de nióbio. Em nosso país, as principais fontes desse metal são jazidas de pirocloro, um mineral que após ser extraído passa por processos de separação magnética e flotação, empregando substâncias como o ácido hexafluorossilícico (H2SiF6) e o ácido clorídrico (HCl), favorecendo o aumento da concentração de pentóxido de nióbio (Nb2O5).
Nos compostos: H2SiF6, HCl e Nb2O5, os números de oxidação dos átomos de Si, Cl e Nb são, respectivamente:
Provas
Caderno Container