Foram encontradas 35.976 questões.
As funções orgânicas desempenham um papel central na determinação das propriedades físicas, químicas e biológicas dos compostos moleculares. Entre essas funções, os grupos carbonila (C=O), presentes em diversas subclasses como aldeídos, cetonas, ácidos carboxílicos, ésteres e amidas, destacam-se por sua versatilidade reacional e amplo espectro de aplicações tecnológicas e biomédicas. Sobre as funções orgânicas com grupos carbonilas, assinale a alternativa INCORRETA. Para responder à questão, considere a figura abaixo:
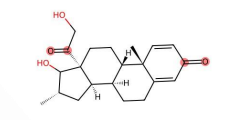
Figura 5 – Estrutura química do cortisol
Provas
Durante o estudo cinético da reação entre o heptanoato de etila (C₉H₁₈O₂) e o íon hipoclorito (ClO⁻) em meio aquoso, os dados experimentais obtidos foram os seguintes:
| [Heptanoato de etila] (mol·L-1) |
[ClO-] (mol·L-1) | Velocidade inicial (mol·L-1·s-1) |
|---|---|---|
| 0,050 | 0,050 | 1,2 × 10-4 |
| 0,100 | 0,050 | 2,4 × 10-4 |
| 0,100 | 0,100 | 4,8 × 10-4 |
Com base nos dados fornecidos, assinale a alternativa que apresenta corretamente a ordem de reação em relação ao heptanoato de etila, ao íon hipoclorito e à ordem global da reação.
Provas
O álcool etílico (etanol) e o éter dimetílico são compostos orgânicos com a mesma fórmula molecular (C2H6O), mas propriedades físicas distintas. Enquanto o etanol é líquido em temperatura ambiente e solúvel em água, o éter dimetílico é um gás e pouco solúvel. Essas diferenças estão relacionadas principalmente devido ao(à):
Provas
O ácido benzoico é um composto orgânico simples, mas amplamente utilizado, conhecido por suas propriedades conservantes e sua presença natural em alguns alimentos. É um composto versátil, com aplicações que vão desde a conservação de alimentos até a síntese de produtos farmacêuticos. Em meio aquoso, ele sofre ionização segundo o seguinte equilíbrio:
C6H5COOH + H2O >≅ H3O+ + C6H5COO-
Considerando o equilíbrio acima e a adição ao sistema de benzoato de sódio, mantendo a temperatura constante, é correto afirmar que o equilíbrio deslocará para a
Provas
Os indicadores ácido-base são substâncias químicas que mudam de cor em resposta à variação do pH de uma solução. Eles são amplamente utilizados em laboratórios, indústrias e até no cotidiano para determinar o ponto final de titulações ou para estimar o pH de um meio. Abaixo, são apresentados dois indicadores e as cores que adquirem em função do pH do meio onde estão inseridos.
| Indicador M | vermelho em pH <2,5 |
| amarelo em pH >3,5 | |
| Indicador B | amarelo em pH <6,0 |
| azul em pH >8,5 |
No laboratório, esses indicadores foram utilizados nas seguintes condições:
I. Solução 0,01 mol/L de HNO3, 100% ionizado.
II. Solução 0,01 mol/L de ácido acético, 1% ionizado.
III. Solução 0,01 mol/L de H2SO4, 100% ionizado.
IV. Solução 0,01 mol/L de NH4OH, 10% ionizada.
Considere que T = 25 °C, Kw = 1,0·10-14 e log2 = 0,3.
De acordo com os dados expostos, assinale a alternativa correta.
Provas
A excelência em trabalhos laboratoriais depende não apenas da execução cuidadosa dos procedimentos, mas também da compreensão das fontes de erro e da aplicação de medidas para neutralizá-las. Somente assim é possível obter dados confiáveis, precisos e exatos, essenciais para conclusões científicas sólidas e decisões baseadas em evidências. Sobre erros que podem afetar os resultados de um experimento, analise as assertivas a seguir:
I. Os erros podem ser reduzidos ao reconhecer e compreender as prováveis fontes de erro e ao adotar protocolos e procedimentos de cálculo apropriados.
II. Uma fonte comum de erro de medição é o descuido, por exemplo, ao ler uma escala na direção incorreta (erro de paralaxe).
III. O uso de um reagente fora da validade para a preparação de uma solução que será utilizada em uma prática pode resultar em um erro aleatório.
Quais estão corretas?
Provas
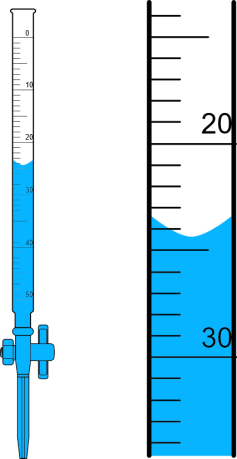
A figura abaixo mostra uma bureta de 50,00 mL e, ao lado, a mesma bureta aumentada para facilitar a medida de volume de líquido contido nela. Considerando os algarismos significativos, assinale a alternativa que apresenta o volume ainda contido nessa bureta.
Provas
A estufa de secagem é amplamente utilizada em laboratórios para remover umidade e resíduos de solventes de vidrarias, garantindo que estejam prontas para uso em procedimentos analíticos sensíveis. No entanto, nem todas as vidrarias podem ser secas em estufa, devido a riscos de deformação, degradação ou perda de calibração. Nesse sentido, assinale a alternativa que apresenta vidrarias que podem ter sua calibração afetada por conta do aquecimento.
Provas
A segurança em um laboratório de química é um aspecto fundamental para garantir a integridade física dos profissionais e estudantes que ali trabalham, bem como a preservação do ambiente e dos equipamentos. Em um espaço onde são manipuladas substâncias potencialmente perigosas, como ácidos, bases, solventes orgânicos e compostos voláteis, a adoção de medidas preventivas é essencial para evitar acidentes. São medidas a serem seguidas em um laboratório:
I. Usar jaleco fechado, de manga longa e com comprimento abaixo do joelho para proteger o corpo e a roupa.
II. Não se deve provar, cheirar ou tocar em produtos químicos diretamente com as mãos.
III. Misturar substâncias ao acaso para avaliar o resultado.
IV. Ao diluir ácidos, colocar primeiro o ácido no recipiente e depois a água.
V. O manuseio de um reagente tóxico e volátil pode ser feito diretamente em uma bancada.
Quais estão corretas?
Provas
A cromatografia é uma das técnicas analíticas mais versáteis e amplamente utilizadas em laboratórios de química, bioquímica, farmácia e meio ambiente. Desenvolvida no início do século XX, a técnica revolucionou a separação, identificação e quantificação de componentes em misturas complexas. Seu princípio fundamental baseia-se na distribuição diferencial dos analitos entre duas fases imiscíveis: uma fase estacionária (sólida ou líquida imobilizada) e uma fase móvel (líquida, gasosa ou supercrítica). Sobre a cromatografia, assinale a alterativa correta.
Provas
Caderno Container