Em um estudo sobre a bioatividade de enzimas que dependem de cofatores metálicos, um bioquímico precisa
preparar um meio reacional onde a concentração de íons magnésio (Mg²⁺) livres seja mantida abaixo de um
determinado limiar para evitar a inibição da enzima. Para isso, ele utiliza uma solução tampão de pH = 9,00 e
adiciona uma fonte de íons magnésio até o exato ponto de saturação, onde se inicia a precipitação do hidróxido
de magnésio (Mg(OH)₂).
Dados de Referência a 25 °C:
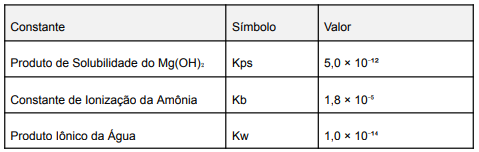
Nessas condições, a concentração máxima de íons magnésio (Mg²⁺) em mol·L⁻¹ que pode ser mantida em solução antes do início da precipitação é:
Dados de Referência a 25 °C:

Nessas condições, a concentração máxima de íons magnésio (Mg²⁺) em mol·L⁻¹ que pode ser mantida em solução antes do início da precipitação é: