Foram encontradas 50 questões.
A diversidade estrutural dos compostos orgânicos nitrogenados confere uma vasta gama de aplicações, desde
a indústria farmacêutica até a produção de polímeros e agroquímicos. A compreensão aprofundada de sua
classificação, isomeria e reatividade é essencial para o desenvolvimento de novas moléculas e processos
sintéticos. Considere a família de aminas com a fórmula molecular C4H11N, que inclui diversos isômeros com
distintas classificações de cadeia carbônica e potencial para isomeria espacial.
Com base na análise dos isômeros da fórmula C4H11N e seus aspectos estruturais e reacionais, a afirmação correta é:
Com base na análise dos isômeros da fórmula C4H11N e seus aspectos estruturais e reacionais, a afirmação correta é:
Provas
Questão presente nas seguintes provas
A decomposição do pentóxido de dinitrogênio (N₂O₅) é uma reação de grande interesse cinético,
frequentemente utilizada para ilustrar mecanismos de reação complexos e a aplicação de aproximações em
química. A reação global é 2N₂O₅(g) → 4NO₂(g) + O₂(g), e sua lei de velocidade experimental é de primeira
ordem em relação a [N₂O₅].
No entanto, o mecanismo proposto para essa reação envolve múltiplas etapas elementares, incluindo a formação de intermediários reativos. Um dos mecanismos mais aceitos é o seguinte:
1. N₂O₅(g) ⇌ NO₂(g) + NO₃(g) (Equilíbrio rápido, k₁ e k₋₁) 2. NO₂(g) + NO₃(g) → NO₂(g) + O₂(g) + NO(g) (Etapa lenta, k₂) 3. NO(g) + NO₃(g) → 2NO₂(g) (Etapa rápida, k₃)
Considerando o mecanismo proposto e aplicando a aproximação do estado estacionário para os intermediários, a lei da velocidade para a decomposição de N₂O₅ é expressa por:
No entanto, o mecanismo proposto para essa reação envolve múltiplas etapas elementares, incluindo a formação de intermediários reativos. Um dos mecanismos mais aceitos é o seguinte:
1. N₂O₅(g) ⇌ NO₂(g) + NO₃(g) (Equilíbrio rápido, k₁ e k₋₁) 2. NO₂(g) + NO₃(g) → NO₂(g) + O₂(g) + NO(g) (Etapa lenta, k₂) 3. NO(g) + NO₃(g) → 2NO₂(g) (Etapa rápida, k₃)
Considerando o mecanismo proposto e aplicando a aproximação do estado estacionário para os intermediários, a lei da velocidade para a decomposição de N₂O₅ é expressa por:
Provas
Questão presente nas seguintes provas
As reações orgânicas são classificadas em diferentes tipos com base nas transformações que ocorrem nas
moléculas. As reações de substituição, adição e eliminação são fundamentais para a síntese de uma vasta
gama de compostos orgânicos, sendo amplamente estudadas e aplicadas em diversos campos da química e
da indústria. A compreensão dos mecanismos envolvidos nessas reações é crucial para prever produtos e
otimizar rotas sintéticas.
Considerando os princípios e características das reações de substituição, adição e eliminação em química orgânica, a opção que apresenta a afirmação correta é:
Considerando os princípios e características das reações de substituição, adição e eliminação em química orgânica, a opção que apresenta a afirmação correta é:
Provas
Questão presente nas seguintes provas
Uma célula galvânica foi construída a 298 K (25 °C), utilizando eletrodos de zinco e cobre, imersos em
soluções de seus respectivos íons, conforme a notação a seguir: Zn(s) | Zn²⁺(aq, 0,01 mol/L) || Cu²⁺(aq, 1,0
mol/L) | Cu(s).
Dados:
● Potencial padrão de redução do Cu²⁺/Cu: E° = +0,34 V ● Potencial padrão de redução do Zn²⁺/Zn: E° = -0,76 V ● Considere a constante de Nernst (RT/F) a 298 K multiplicada por ln(10) como 0,0592 V.
Nessas condições, o potencial medido para a célula é:
Dados:
● Potencial padrão de redução do Cu²⁺/Cu: E° = +0,34 V ● Potencial padrão de redução do Zn²⁺/Zn: E° = -0,76 V ● Considere a constante de Nernst (RT/F) a 298 K multiplicada por ln(10) como 0,0592 V.
Nessas condições, o potencial medido para a célula é:
Provas
Questão presente nas seguintes provas
A polarimetria é uma técnica analítica crucial na indústria sucroalcooleira, utilizada para o controle de qualidade
e a determinação da concentração de açúcares, principalmente a sacarose em diferentes etapas do processo
produtivo. O princípio fundamental desta técnica baseia-se na capacidade de certas substâncias, denominadas
opticamente ativas, de rotacionar o plano da luz polarizada. O esquema a seguir ilustra o funcionamento básico
de um polarímetro, equipamento empregado para medir essa rotação.
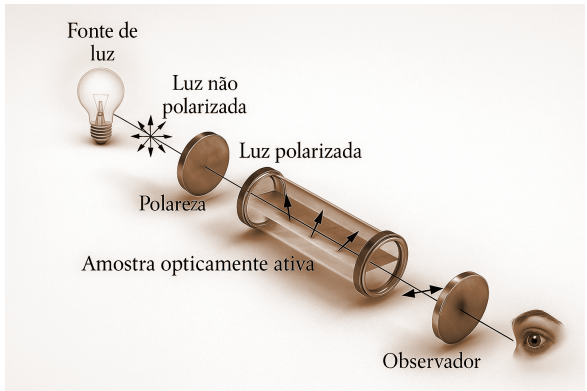
Esquema de aparelhagem para análise polarimétrica (adaptado de Polarimetric Analysis Service, Creative Proteomics, acesso em 22 ago. 2025).
Com base nos princípios da polarimetria e em sua aplicação no contexto da indústria sucroalcooleira, a opção que apresenta a afirmação correta é:

Esquema de aparelhagem para análise polarimétrica (adaptado de Polarimetric Analysis Service, Creative Proteomics, acesso em 22 ago. 2025).
Com base nos princípios da polarimetria e em sua aplicação no contexto da indústria sucroalcooleira, a opção que apresenta a afirmação correta é:
Provas
Questão presente nas seguintes provas
A figura a seguir representa uma pilha eletroquímica de cobre e prata (Pilha Ag/Cu), composta por dois
eletrodos imersos em soluções de seus respectivos íons na concentração de 1,0 mol/L, conectados por um
voltímetro e uma ponte salina. Este arranjo permite a conversão de energia química em energia elétrica por
meio de reações de oxirredução espontâneas.
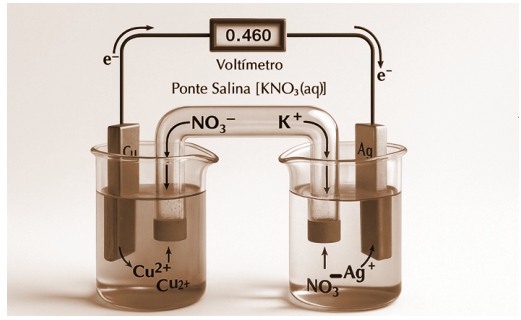
Representação esquemática de uma pilha Cu–Ag (adaptado de Eletroquímica, Instituto de Química – USP, p. 34, disponível em: https://www.iq.usp.br/fmvichi/html/Eletroquimica.pdf, acesso em: 21 ago. 2025. Baseado em Pearson Prentice Hall, 2007).
Com base na análise da Pilha Ag/Cu apresentada na figura e nos princípios da eletroquímica, assinale a opção que apresenta a afirmação correta.

Representação esquemática de uma pilha Cu–Ag (adaptado de Eletroquímica, Instituto de Química – USP, p. 34, disponível em: https://www.iq.usp.br/fmvichi/html/Eletroquimica.pdf, acesso em: 21 ago. 2025. Baseado em Pearson Prentice Hall, 2007).
Com base na análise da Pilha Ag/Cu apresentada na figura e nos princípios da eletroquímica, assinale a opção que apresenta a afirmação correta.
Provas
Questão presente nas seguintes provas
O processo de biotransformação de fármacos no organismo humano frequentemente envolve reações de
oxidação e redução catalisadas por enzimas do citocromo P450. Considere a oxidação de um álcool primário a
ácido carboxílico e a redução de uma cetona a álcool secundário. Essas transformações são cruciais para a
alteração da polaridade e a consequente eliminação ou ativação de compostos orgânicos.
Em relação às reações de oxidação e redução em química orgânica, e considerando os exemplos mencionados, assinale a opção correta.
Em relação às reações de oxidação e redução em química orgânica, e considerando os exemplos mencionados, assinale a opção correta.
Provas
Questão presente nas seguintes provas
Um professor de química planeja o preparo de soluções para uma aula prática de titulação ácido-base. Serão
preparadas uma solução de hidróxido de sódio (NaOH) com concentração de 0,2 mol/L e uma solução de ácido
clorídrico (HCl) com concentração de 0,1 mol/L. O NaOH é um reagente sólido de alta pureza, enquanto o HCl
é fornecido como uma solução aquosa concentrada.
Dados de Referência:
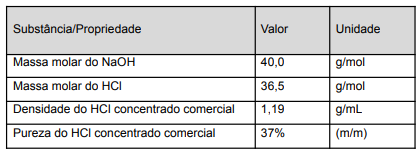
Para o preparo de 500 mL de cada uma dessas soluções, a massa de NaOH necessária e o volume de HCl concentrado a ser utilizado, respectivamente, são:
Dados de Referência:

Para o preparo de 500 mL de cada uma dessas soluções, a massa de NaOH necessária e o volume de HCl concentrado a ser utilizado, respectivamente, são:
Provas
Questão presente nas seguintes provas
A acidez de um composto orgânico, quantificada pelo seu pKa, é profundamente influenciada por efeitos
eletrônicos que estabilizam sua base conjugada. O efeito indutivo, resultante da polarização de ligações σ por
grupos eletronegativos e o efeito de ressonância, que deslocaliza a carga negativa através de um sistema π,
são determinantes. Considere os quatro ácidos carboxílicos a seguir, cujas estruturas são bem estabelecidas
na literatura química.
Compostos:
I. Ácido acético (CH₃COOH) II. Ácido cloroacético (ClCH₂COOH) III. Ácido tricloroacético (Cl₃CCOOH) IV. Ácido benzóico (C₆H₅COOH)
A ordem crescente de acidez para estes compostos, justificada pela análise dos efeitos eletrônicos que atuam sobre a estabilidade de suas respectivas bases conjugadas, é:
Compostos:
I. Ácido acético (CH₃COOH) II. Ácido cloroacético (ClCH₂COOH) III. Ácido tricloroacético (Cl₃CCOOH) IV. Ácido benzóico (C₆H₅COOH)
A ordem crescente de acidez para estes compostos, justificada pela análise dos efeitos eletrônicos que atuam sobre a estabilidade de suas respectivas bases conjugadas, é:
Provas
Questão presente nas seguintes provas
Em um estudo sobre a bioatividade de enzimas que dependem de cofatores metálicos, um bioquímico precisa
preparar um meio reacional onde a concentração de íons magnésio (Mg²⁺) livres seja mantida abaixo de um
determinado limiar para evitar a inibição da enzima. Para isso, ele utiliza uma solução tampão de pH = 9,00 e
adiciona uma fonte de íons magnésio até o exato ponto de saturação, onde se inicia a precipitação do hidróxido
de magnésio (Mg(OH)₂).
Dados de Referência a 25 °C:
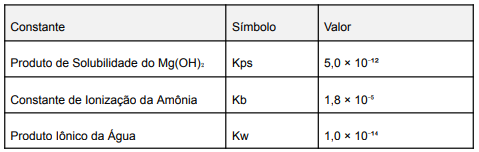
Nessas condições, a concentração máxima de íons magnésio (Mg²⁺) em mol·L⁻¹ que pode ser mantida em solução antes do início da precipitação é:
Dados de Referência a 25 °C:

Nessas condições, a concentração máxima de íons magnésio (Mg²⁺) em mol·L⁻¹ que pode ser mantida em solução antes do início da precipitação é:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container