Em 1909 Fritz Haber e seu assistente Robert Le
Rossignol demonstraram seu processo de produzir amônia
a partir de nitrogênio do ar e prover, desse modo, uma
fonte abundante de compostos para a agricultura e para os
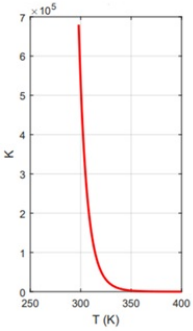
armamentos. O gráfico a seguir relaciona a temperatura
(em Kelvin) com os valores da constante de equilíbrio (K)
para a reação de síntese de amônia.
N2(g) + 3 H2(g) ⇆ 2 NH3(g)
Leia as afirmativas a seguir:
I- A produção de amônia será reduzida com o aumento da temperatura.
II- A reação é endotérmica no sentido direto da reação.
III- A constante de equilíbrio em termos de pressões parciais é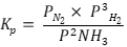
IV- A velocidade da reação será aumentada com o aumento da temperatura.
V- A adição de mais N à reação desloca o equilíbrio para a direita, produzindo mais amônia.
É CORRETO o que se afirma em:
N2(g) + 3 H2(g) ⇆ 2 NH3(g)

Leia as afirmativas a seguir:
I- A produção de amônia será reduzida com o aumento da temperatura.
II- A reação é endotérmica no sentido direto da reação.
III- A constante de equilíbrio em termos de pressões parciais é
IV- A velocidade da reação será aumentada com o aumento da temperatura.
V- A adição de mais N à reação desloca o equilíbrio para a direita, produzindo mais amônia.
É CORRETO o que se afirma em: