Foram encontradas 60 questões.
Titulação volumétrica é o processo de adição de
volumes discretos de um reagente, geralmente com o
auxílio de uma bureta, para quantificar o analito na
amostra.
As afirmativas I, II, III e IV relacionam-se com as
características e uso das buretas.
I. Consistem de um tubo cilíndrico uniformemente calibrado em toda sua extensão de escala e possuem uma torneira na sua extremidade inferior.
II. A lubrificação dificulta o manuseio de buretas cujas torneiras são de vidro esmerilhado.
III. Recomenda-se verificar a presença de bolhas de ar retidas no seu interior, antes de iniciar a análise.
IV. A leitura do menisco é feita de forma relativa, sempre considerando a parte inferior do menisco.
Assinale a alternativa em que (todas) a(s) afirmativa(s) está(ão) CORRETA(S):
I. Consistem de um tubo cilíndrico uniformemente calibrado em toda sua extensão de escala e possuem uma torneira na sua extremidade inferior.
II. A lubrificação dificulta o manuseio de buretas cujas torneiras são de vidro esmerilhado.
III. Recomenda-se verificar a presença de bolhas de ar retidas no seu interior, antes de iniciar a análise.
IV. A leitura do menisco é feita de forma relativa, sempre considerando a parte inferior do menisco.
Assinale a alternativa em que (todas) a(s) afirmativa(s) está(ão) CORRETA(S):
Provas
Questão presente nas seguintes provas
Considere que um técnico em química preparou uma
solução de NaOH 0,100 mol/L e padronizou-a utilizando o
biftalato de potássio (KHC8H4O4) e fenolftaleína como
indicador. Na Tabela a seguir encontram-se as medidas de
massa de biftalato de potássio e as medidas de volume
gasto de NaOH 0,100 mol/L, obtidas pelo técnico, para a
triplicata de análise.

Dados: equação da reação: NaOH(aq) + HOOCC6H4COOK(aq) → NaOOCC6H4COOK(aq) + H2O(liq) NaOH = 40,00 g/mol; KHC8H4O4 = 204, 2 g/mol
Considerando a análise realizada, assinale a alternativa que apresenta a concentração média (C) da solução de NaOH, o seu fator de correção (FC), o titulado e o titulante, respectivamente.

Dados: equação da reação: NaOH(aq) + HOOCC6H4COOK(aq) → NaOOCC6H4COOK(aq) + H2O(liq) NaOH = 40,00 g/mol; KHC8H4O4 = 204, 2 g/mol
Considerando a análise realizada, assinale a alternativa que apresenta a concentração média (C) da solução de NaOH, o seu fator de correção (FC), o titulado e o titulante, respectivamente.
Provas
Questão presente nas seguintes provas
Na Titulação de Neutralização são utilizadas
substâncias indicadoras que sinalizam o ponto final da
análise, em função da mudança da cor devida à mudança
de pH do meio. Sobre os indicadores assinale a alternativa
CORRETA:
Provas
Questão presente nas seguintes provas
Ao medirmos o pH de uma solução salina, em muitos
casos não encontraremos o valor “neutro” (pH = 7,0), e sim
valores de pH< 7,0 ou pH>7. Este comportamento pode ser
explicado pela Teoria ácido-base de Bronsted-Löwry que
afirma que o íon pode ser um ácido ou uma base. Durante
uma aula experimental de química, o professor pediu para
que os alunos preparassem 5 soluções salinas, de
concentração 0,100 mol/L, utilizando água destilada e
cada um dos sais a seguir.
I. Iodeto de sódio
II. Brometo de amônio
III. Cianeto de potássio
IV. Fluoreto de amônio
V. Acetato de metilamônio
Dados: Constantes de Acidez e de Basicidade em temperatura igual 25 °C:

Assinale a alternativa que apresenta os sais que produzirão soluções com valores de pH<7.
I. Iodeto de sódio
II. Brometo de amônio
III. Cianeto de potássio
IV. Fluoreto de amônio
V. Acetato de metilamônio
Dados: Constantes de Acidez e de Basicidade em temperatura igual 25 °C:

Assinale a alternativa que apresenta os sais que produzirão soluções com valores de pH<7.
Provas
Questão presente nas seguintes provas
Deseja-se preparar 500,00 mL de solução de ácido
clorídrico 0,150 mol/L. Sabe-se que o frasco estoque do
ácido contém 37,0 % em massa e densidade de 1,20
g/cm . O volume, em mililitros, a ser retirado do frasco
estoque para o preparo da solução é
Dado: HCl = 36,5 g/mol
Dado: HCl = 36,5 g/mol
Provas
Questão presente nas seguintes provas
Em 1909 Fritz Haber e seu assistente Robert Le
Rossignol demonstraram seu processo de produzir amônia
a partir de nitrogênio do ar e prover, desse modo, uma
fonte abundante de compostos para a agricultura e para os
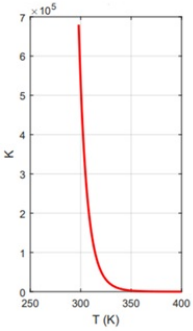
armamentos. O gráfico a seguir relaciona a temperatura
(em Kelvin) com os valores da constante de equilíbrio (K)
para a reação de síntese de amônia.
N2(g) + 3 H2(g) ⇆ 2 NH3(g)
Leia as afirmativas a seguir:
I- A produção de amônia será reduzida com o aumento da temperatura.
II- A reação é endotérmica no sentido direto da reação.
III- A constante de equilíbrio em termos de pressões parciais é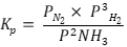
IV- A velocidade da reação será aumentada com o aumento da temperatura.
V- A adição de mais N à reação desloca o equilíbrio para a direita, produzindo mais amônia.
É CORRETO o que se afirma em:
N2(g) + 3 H2(g) ⇆ 2 NH3(g)

Leia as afirmativas a seguir:
I- A produção de amônia será reduzida com o aumento da temperatura.
II- A reação é endotérmica no sentido direto da reação.
III- A constante de equilíbrio em termos de pressões parciais é
IV- A velocidade da reação será aumentada com o aumento da temperatura.
V- A adição de mais N à reação desloca o equilíbrio para a direita, produzindo mais amônia.
É CORRETO o que se afirma em:
Provas
Questão presente nas seguintes provas
Após a filtração, um precipitado gravimétrico é
aquecido até que sua massa se torne constante. Esse
procedimento remove o solvente e qualquer espécie volátil
arrastada com o precipitado. Em algumas situações os
precipitados também são calcinados para decompor o
sólido e para formar um composto de composição
conhecida.
Fonte: SKOOG, D.; WEST, D.; HOLLER, F. J. e CROUCH, S. Fundamentos de Química Analítica. Tradução da 9. ed. Norte-Americana. São Paulo: Cengage Learning, 2014.
Sobre os processos de secagem e calcinação, podemos afirmar, exceto:
Fonte: SKOOG, D.; WEST, D.; HOLLER, F. J. e CROUCH, S. Fundamentos de Química Analítica. Tradução da 9. ed. Norte-Americana. São Paulo: Cengage Learning, 2014.
Sobre os processos de secagem e calcinação, podemos afirmar, exceto:
Provas
Questão presente nas seguintes provas
É possível determinar níquel (Ni) com dimetilglioxima
(DMG) em amostras de sal através da precipitação do
níquel como um complexo vermelho-alaranjado de DMG,
que é então filtrado, seco e pesado. Considere que um
analista pesou uma massa de 0,2930 g de uma amostra de
sal. Na etapa de filtração foi utilizado um papel de filtro
faixa preta de massa igual a 0,8787 g. Após as etapas de
filtração, lavagem e secagem, a massa medida do papel
de filtro foi igual a 1,1676 g.
Qual é a porcentagem de Ni na amostra?
Dados: dimetilglioximato de níquel - Ni[C4H6(NOH)(NO)]2 = 288,9 g/mol, Ni - 58,6 g/mol.
Qual é a porcentagem de Ni na amostra?
Dados: dimetilglioximato de níquel - Ni[C4H6(NOH)(NO)]2 = 288,9 g/mol, Ni - 58,6 g/mol.
Provas
Questão presente nas seguintes provas
As reações que envolvem a transferência de elétrons
de uma substância para outra são chamadas de reações
redox. Todas as reações a seguir são do tipo redox,
EXCETO:
Provas
Questão presente nas seguintes provas
Isômeros estruturais são compostos que possuem a
mesma fórmula molecular, mas diferem na forma como
seus átomos estão conectados. Essa diferença na
estrutura resulta em propriedades físicas e
químicas distintas. A tabela a seguir apresenta a
temperatura de ebulição de três isômeros estruturais.
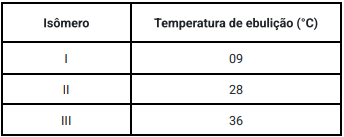
Fonte: BROWN, T. L.; LEMAY, Jr. H. E.; BURSTEN, B. E.; MURPHY, C. J.; WOODWARD, P. M. e STOLTZFUS, M. W. Química: A Ciência Central. Tradução da 13. ed. NorteAmericana. São Paulo: Pearson, 2016.
Assinale a alternativa que identifica corretamente os isômeros I, II e III, respectivamente.

Fonte: BROWN, T. L.; LEMAY, Jr. H. E.; BURSTEN, B. E.; MURPHY, C. J.; WOODWARD, P. M. e STOLTZFUS, M. W. Química: A Ciência Central. Tradução da 13. ed. NorteAmericana. São Paulo: Pearson, 2016.
Assinale a alternativa que identifica corretamente os isômeros I, II e III, respectivamente.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container