No século XIX, cientistas observaram que o comportamento e a descrição do átomo de Dalton não se enquadravam no sistema newtoniano de princípios físicos e não explicavam o comportamento elétrico da matéria. Uma das linhas de investigação consistiu em aplicar descargas elétricas em um tubo que continha gás em pequena quantidade e em observar as emissões eletromagnéticas irradiadas, capazes de produzir fluorescência na incidência em certos materiais. Descobriu-se, depois, que a frequência das emissões chamadas de raios X era proporcional ao número atômico (Z) do átomo emissor, segundo a equação de Moseley,\( f = (2,47 \times 10^{15} \times (Z-1)^2 \), em que \( f \) representa a frequência de emissão relativa às transições eletrônicas ocorridas na camada eletrônica K desse átomo, em Hertz. A figura a seguir mostra o espectro de emissão de raios X proveniente do bombardeamento de um feixe de elétrons em determinado alvo metálico.
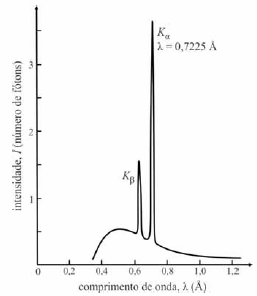
A energia relativa à emissão K\( _\beta \) é maior que a relacionada à emissão \( _\alpha \), ambas mostradas na figura.