Disciplina: Engenharia Química
Banca: OBJETIVA
Orgão: Pref. Santa Maria-RS
Considerar a reação química reversível hipotética a seguir, a qual se processa isotermicamente a 25ºC:
aA(g) !$ \Leftrightarrow, !$ cC(g)
Na figura abaixo é apresentado o gráfico de entalpia da reação com e sem catalisador. Considerar que para a reação, a variação de entropia (!$ \Delta !$Sº) é igual a -130J/(K.mol).
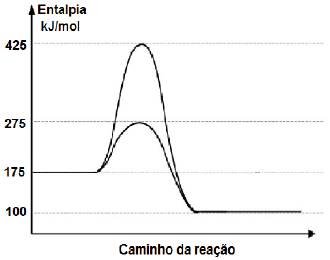
Sobre essa reação, analisar os itens abaixo:
I. A adição do catalisador desloca o equilíbrio da reação para o lado da formação de A.
II. O aumento da temperatura favorece a formação dos produtos.
III. A energia de Gibbis para a reação catalisada é maior que 35kJ/mol.
IV. Na reação balanceada, se a > c, então o aumento da pressão desloca o equilíbrio para o lado da formação de C.
Está(ão) CORRETO(S):