Um estudante do IFMS montou uma cela galvânica (pilha) conforme esquema a seguir:
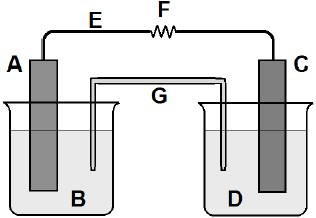
Legenda da figura: (A) placa de estanho, (B) solução aquosa contendo íons Sn2+, (C) placa de alumínio, (D) solução aquosa contendo íons Aℓ3+, (E) fio metálico, (F) resistência elétrica e (G) ponte salina.
Considerando os seguintes dados:
Eº(Sn2+/Sn) = -0,14 V
Eº(Aℓ3+/Aℓ) = -1,68 V
Durante o funcionamento da pilha, o estudante fez algumas afirmações:
I. A concentração de íons alumínio aumenta na solução da direita (D).
II. Na placa de alumínio ocorre a corrosão.
III. O fluxo de elétrons ocorre pelo fio metálico a partir da placa de estanho em direção à placa de alumínio.
IV. Na placa de estanho ocorre a redução.
V. A placa de estanho é o polo negativo da cela galvânica.
Dessas afirmações,