Foram encontradas 25 questões.
A Teoria dos Orbitais Moleculares (TOM) é uma ferramenta útil na descrição de ligações químicas, na avaliação da estabilidade química e na previsão de propriedades físicas das moléculas como absorção de luz e magnetismo. Utilizando o conceito de ordem de ligação (OL) [OL = (EOL - EOAL) / 2 ], em que EOL é o número de elétrons em orbitais ligantes e EOAL é o número de elétrons em orbitais antiligantes, é possível avaliar qualitativamente a estabilidade de uma determinada molécula. Abaixo segue o diagrama de orbitais moleculares para o óxido nítrico (NO), que no estado gasoso é uma molécula paramagnética.
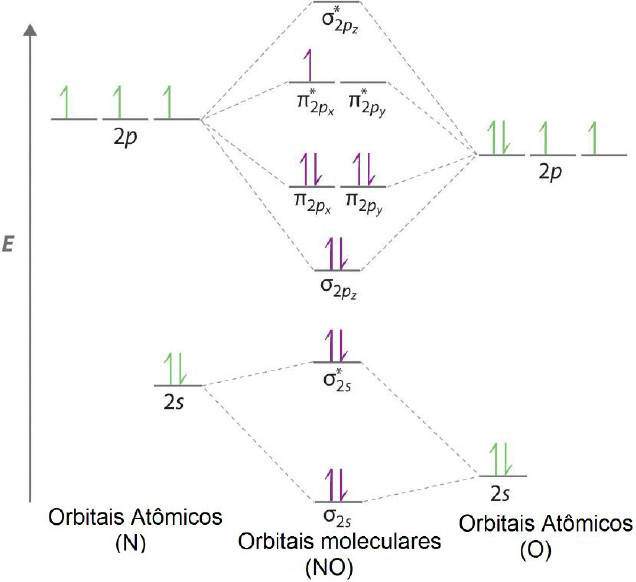
Disponível em <https://chemistry.stackexchange.com/questions/15315/nitric-oxide-dimerization> Acesso em 8 mar. 2019.
Sendo assim, escolha a alternativa que representa quais características serão apresentadas no íon NO+.
Provas
Um estudante do IFMS montou uma cela galvânica (pilha) conforme esquema a seguir:
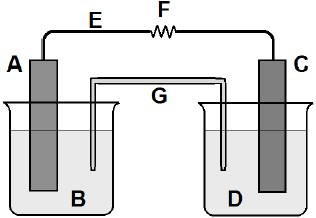
Legenda da figura: (A) placa de estanho, (B) solução aquosa contendo íons Sn2+, (C) placa de alumínio, (D) solução aquosa contendo íons Aℓ3+, (E) fio metálico, (F) resistência elétrica e (G) ponte salina.
Considerando os seguintes dados:
Eº(Sn2+/Sn) = -0,14 V
Eº(Aℓ3+/Aℓ) = -1,68 V
Durante o funcionamento da pilha, o estudante fez algumas afirmações:
I. A concentração de íons alumínio aumenta na solução da direita (D).
II. Na placa de alumínio ocorre a corrosão.
III. O fluxo de elétrons ocorre pelo fio metálico a partir da placa de estanho em direção à placa de alumínio.
IV. Na placa de estanho ocorre a redução.
V. A placa de estanho é o polo negativo da cela galvânica.
Dessas afirmações,
Provas
O álcool coniferílico tem fórmula molecular igual a C10H12O3. O composto pode ser isolado de pinheiros, sendo um intermediário na biossíntese de eugenol e dos estilbenoides e da cumarina. Uma solução de Br2 em CCl4 é descorada quando adicionada ao álcool coniferílico que forma A (C10H12O3Br2). Após ozonólise redutiva, o álcool coniferílico produz vanilina (4-hidroxi-3-metoxibenzaldeído) e B (C2H4O2). Diante do exposto, assinale a alternativa que apresenta a fórmula estrutural correta para o álcool coniferílico.
Provas
A energia dos orbitais atômicos, dentre outros fatores, está relacionada com a capacidade de interação dos elétrons com o seu núcleo. Em um dado átomo polieletrônico, observa-se experimentalmente por medidas espectroscópicas que o orbital 2s possui energia menor que o orbital 2p. Esse comportamento pode ser compreendido observando o gráfico abaixo de probabilidade radial para os orbitais 1s, 2s e 2p.
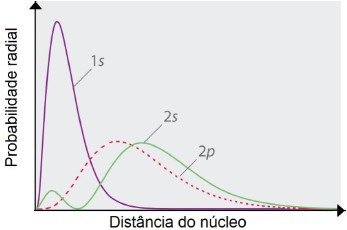
Adaptado de: <https://2012books.lardbucket.org/books/principles-of-general-chemistry-v1.0/s10-05-atomic-orbitals-and-their-ener.html>. Acesso em 08 mar. 2019.
Sendo assim, analise as afirmações a seguir e assinale a alternativa correta:
I. Os orbitais 2s e 2p são degenerados.
II. Os orbitais 2s têm uma maior capacidade de penetração do que os orbitais 2p.
III. Os orbitais 2p são menos blindados pelos elétrons dos orbitais 1s, quando comparados aos orbitais 2s.
IV. Um átomo com configuração eletrônica terminada em ns1 tem menor energia de ionização quando comparado a um outro átomo com configuração eletrônica terminada em ns2np1.
Provas
A maioria das proteínas existe apenas em duas formas: a nativa e a desdobrada, quando são termicamente ou quimicamente desnaturadas. Não são comuns concentrações apreciáveis de outros intermediários estáveis em equilíbrio com as formas nativa e desdobrada. Para essas proteínas, o processo de dobramento-desdobramento pode ser tratado como um sistema em equilíbrio químico.
Dessa forma, qual é a constante de equilíbrio para o referido processo quando os estados nativo e desnaturado estão presentes em proporções iguais no equilíbrio a 298K?
Provas
No livro A Paixão Segundo G.H., de Clarice Lispector, é encontrada a seguinte citação: “O nó vital é um dedo apontando-o – e, aquilo que foi apontado, desperta como um miligrama de radium no escuro tranquilo”. Considerando que o tempo de meia-vida do isótopo citado por Clarice corresponde a 12 dias, determine a quantidade de radium que restará após 2 meses.
Provas
O controle do pH é crucial para a capacidade de sobrevivência de organismos vivos, porque até mesmo pequenas variações de pH podem provocar mudanças na forma das enzimas e perda da sua função.
(Atkins, P.W.; Jones, L. Princípios de Química: Questionando a Vida Moderna e o Meio Ambiente. Ed. 5, Bookman, 2011.)
Dessa forma, assinale a alternativa correta:
Provas
Considere uma reação hipotética com três reagentes (A, B e C) e um produto (D). A velocidade de formação de D foi monitorada em quantidades diferentes dos reagentes, conforme a tabela abaixo:
| Experimento | [A] mol.L-1 | [B] mol.L-1 | [C] mol.L-1 | Velocidade de formação de D mol.L-1.s-1 |
| I | x | 2y | z | v |
| II | 2x | y | z | 2v |
| III | 2x | 2y | z | 4v |
| IV | 2x | 2y | 3z | 108v |
Determine a velocidade da reação em função de v se as concentrações de A, B e C, forem, respectivamente, igual a: 3x, 5y e 2z.
Provas
Titulações envolvem a adição de uma solução, chamada titulante, colocada em uma bureta, a uma solução que contém amostra, chamada de analito, colocada em Erlenmeyer. Por exemplo, se um químico ambiental estivesse estudando o escoamento de resíduos de uma mina e precisasse conhecer a concentração de ácido na água uma amostra de efluentes da mina seria o analito e uma solução básica de concentração conhecida seria o titulante.
(Atkins, P.W.; Jones, L. Princípios de Química: Questionando a Vida Moderna e o Meio Ambiente. Ed 5, Bookman, 2011.)
Sobre titulação, assinale a alternativa correta:
Provas
No livro Desespero, de Stephen King, um dos personagens faz a seguinte afirmação: “A gente tira o cobre da terra com ácido sulfúrico. A melhor maneira de aplicar é com esguichos... parecem grandes molhadores de grama.”
Considerando que uma amostra de 2,0 kg, contendo 80% de óxido de cobre II, foi utilizada para reagir com o ácido citado no livro de Stephen King. Admitindo que os outros compostos da amostra não reagem com o ácido, determine a massa aproximada de ácido necessária para que todo o cobre da amostra sofra reação química.
Considere as seguintes massas molares em g.mol-1: Cu = 63,5; O = 16; H = 1 e S = 32.
Provas
Caderno Container