Julgue o item a seguir.
2NaI(s) + MnO2(s) + 3H2SO4(aq) 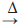 2NaHSO4(aq) + MnSO4(aq) + 2H2O(!$ \ell !$) + I2(g)
2NaHSO4(aq) + MnSO4(aq) + 2H2O(!$ \ell !$) + I2(g)
O iodo gasoso, I2(g), pode ser obtido em laboratório pelo aquecimento da mistura de iodeto de sódio, NaI(s), e dióxido de manganês, MnO2(s), com gotejamento contínuo de ácido sulfúrico concentrado, H2SO4(aq), de acordo com a reação representada, de maneira simplificada, pela equação química.
A equação de oxirredução representada revela que o iodeto de sódio atua como agente oxidante porque cada átomo de iodo do iodeto de sódio transfere um elétron para o átomo de manganês do dióxido de manganês.