Foram encontradas 85 questões.
Julgue o item a seguir.
A coleta de amostras sólidas do solo envolve a retirada de material homogêneo da superfície terrestre, o qual, posteriormente, é usado diretamente na determinação analítica.
Provas
Julgue o item a seguir.
A separação dos componentes de uma mistura por cromatografia em camada delgada, CCD, é uma técnica rápida, que tem várias aplicações em química orgânica e necessita de uma quantidade muito pequena de amostra.
Provas
Julgue o item a seguir.

Considerando-se o esquema que representa os componentes básicos de um espectrômetro, é correto afirmar que a fonte de energia eletromagnética precisa fornecer radiação estável, com intensidade constante, e que, para a análise de uma amostra, um determinado comprimento de onda, λ, precisa ser selecionado do espectro fornecido pela fonte.
Provas
Julgue o item a seguir.
A lei de Lambert-Beer, que relaciona a absorção de uma espécie química, A, à absortividade molar, ε; ao comprimento de onda do trajeto, b; à concentração da solução, C, expressa na equação A = ε b C, indica que a concentração da espécie em análise é inversamente proporcional à absorbância.
Provas
Julgue o item a seguir.
A semirreação representada por Hg2Cl2 + 2e– → 2Hg + 2Cl– E0 = 0,2676V(a 25ºC), que ocorre na semicela do eletrodo de calomelano, indica que a redução do Hg2+ 2 para Hg0 ocorre de maneira espontânea.
Provas
Julgue o item a seguir.
O Eletrodo de Hidrogênio é largamente utilizado na potenciometria porque é um eletrodo de referência secundária de fácil construção e manuseio.
Provas
Julgue o item a seguir.
CURVA DE TITULAÇÃO DE UMA SOLUÇÃO DE ÁCIDO ACÉTICO COM SOLUÇÃO PADRÃO DE HIDRÓXIDO DE SÓDIO
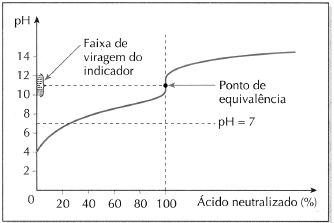
O argumento que justifica o ponto de equivalência correspondente ao pH acima de 7, na padronização de uma solução de ácido acético com uma solução de hidróxido de sódio, como apresentado no gráfico, é a hidrólise de íons acetato, CH3COO–(aq), um dos produtos da reação entre o ácido acético e o hidróxido de sódio.
Provas
Julgue o item a seguir.
A padronização de 200mL de uma solução de ácido sulfúrico consumiu 100mL de solução de hidróxido de sódio 0,5mol L–1; nesse caso, pode-se concluir que a concentração da solução de ácido sulfúrico é 9,8g L–1.
Provas
Julgue o item a seguir.
A substância química cuja análise revelou a presença de 49,5% de carbono, 5,15% de hidrogênio, 28,9% de nitrogênio, 16,5% de oxigênio, percentual em massa, e massa molar, aproximadamente, 195g mol–1 é representada pela fórmula molecular C8H10N4O2.
Provas
Julgue o item a seguir.
Uma amostra de 50,0mL de solução de oxalato de cálcio, CaC2O4(aq), substância encontrada nas folhas de espinafre e nas sementes de tomate, constituída por 0,5250g desse sal, apresenta, aproximadamente, 4,1.10-3mol de íons oxalato.
Provas
Caderno Container