O gráfico qualitativo abaixo ilustra a relação da energia livre de Gibbs molar !$ (G_m) !$ de uma substância pura com a temperatura !$ (T) !$ em seus estados sólido, líquido e gasoso.
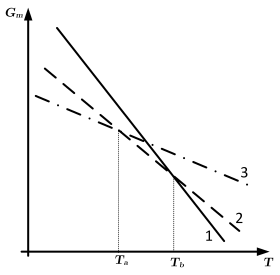
Considere as afirmativas abaixo:
I. As três retas são decrescentes, pois a expressão !$ G_m = H_m - TS_m !$ é representada por uma reta com inclinação definida pelo termo !$ (-S_m) !$.
II. As retas 1, 2 e 3 representam a substância nos estados sólido, líquido e gasoso, respectivamente.
III. A temperatura !$ T_a !$ indica o ponto de fusão da substância nas condições em que o gráfico foi obtido.
IV. Em temperaturas mais altas do que !$ T_b !$, a fase 1 da substância é a mais estável.
Assinale as alternativas que são verdadeiras.