A reação de decomposição do peróxido de hidrogênio, !$ H_2O_2 !$, catalisado com o cloreto férrico, !$ FeCl_3 !$, segue uma lei de velocidade simples de reação de primeira ordem.
A cinética dessa reação foi acompanhada para uma amostra de água oxigenada com uma concentração inicial de 1 mol !$ L^{-1} !$ e a uma temperatura constante de 25 ºC. Água oxigenada é uma solução aquosa de peróxido de hidrogênio. Nesse experimento, a quantidade de peróxido de hidrogênio presente em um tempo escolhido t foi determinada através de titulações com permanganato de potássio, !$ KMnO_4 !$, de alíquotas de 5 mL de solução acidificada de água oxigenada. Os resultados obtidos são mostrados na tabela abaixo.
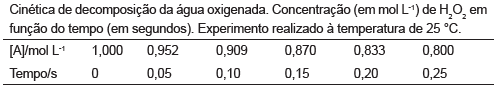
Com os dados apresentados acima e seus conhecimentos básicos de processos cinéticos, podemos afirmar que:
1. A velocidade média desta reação no intervalo de 0,10 s a 0,15 s é -0,78 mol !$ L^{-1} !$ !$ S^{-1} !$ .
2. A velocidade da reação de decomposição da água oxigenada diminui a medida que o tempo aumenta.
3. Utilizando-se as mesmas condições iniciais para a concentração da água oxigenada, a velocidade de reação de decomposição catalisada com !$ FeCl_3 !$ seria idêntica para um experimento conduzido à tempertura de 42º C.
4. A velocidade dessa reação química não deve alterar-se se ions iodeto !$ I^- !$ são utilizados como catalisador em lugar do !$ FeCl_3 !$.
Dessas, são VERDADEIRAS as afirmativas: