Considere os dois sistemas fechados a seguir, contendo um gás ideal. Ambos passarão por um processo de aquecimento e receberão a mesma quantidade de calor Q, sendo que o processo no sistema da esquerda ocorrerá dentro de um sistema rígido a volume constante, enquanto que o processo no sistema da direita ocorrerá a uma pressão constante dentro de um cilindro-pistão (fronteira superior pode se mover livremente).
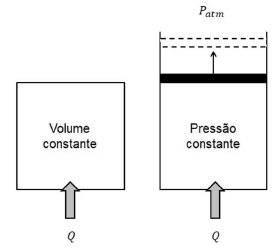
Fonte: Próprio autor.
Com base nos conceitos da primeira lei da termodinâmica (!$ \Delta U = Q+W) !$), que diz que uma variação de energia interna (U) em um sistema fechado é igual à soma do calor (Q) e do trabalho (W), analise as afirmativas a seguir.
I. O sistema a volume constante apresentará uma maior variação de temperatura, já que a variação da energia interna será maior.
II. O sistema a pressão constante não exercerá trabalho sobre a vizinhança, já que apenas a pressão atmosférica irá se contrapor ao movimento do pistão.
III. O calor recebido pelo sistema a pressão constante se converterá apenas em aumento de volume do gás, e o processo será isotérmico, tendo em vista que o pistão pode se mover livremente.
Está(ão) correta(s) a(s) afirmativa(s)