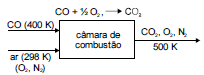
Em uma câmara de combustão, 1 kmol de CO disponível a 400 K é queimado completamente com 20% de excesso de ar, que é injetado na câmara a 298 K, conforme ilustra o esquema acima. Os gases de combustão saem da câmara de combustão a 500 K e 1 atm de pressão. Considere que a entalpia-padrão de combustão do CO, a 298 K, seja de -283 kJ/mol, que o ar seja composto por 20% de O2 e 80% de N2 (em quantidade de matéria) e que a capacidade calorífica à pressão constante do CO2 não varie entre 298 K e 300 K. Na tabela abaixo são informadas as entalpias molares de alguns gases !$ (\hat {H}º), !$ a 1 atm de pressão, para diferentes temperaturas, tendo como referência a temperatura de 298 K.
|
temperatura (K) |
!$ (\hat {H}º) !$ (J/mol) | |||
|
N2 |
O2 | CO |
CO2 |
|
|
298 |
0 | 0 | 0 | 0 |
| 300 | 58 | 58 | 58 | 74 |
| 400 | 2.967 | 3.020 | 2.971 |
3.991 |
| 500 | 5.916 | 6.079 | 5.924 |
8.292 |
Com base na situação descrita, nas considerações feitas e nos dados fornecidos, julgue o item que se seguem.
A energia térmica liberada na câmara de combustão é menor que 200 MJ.