Em um laboratório de química, são realizadas, diariamente, diversas análises químicas para determinação de inúmeras substâncias. Suponha que você está determinando uma curva de calibração com uma solução padrão de sulfato de cobre a 0,1 mol.L-1. Inicialmente foram diluídas para que as concentrações dos analitos de interesse estivessem dentro da faixa de linearidade da curva de calibração, como mostra a tabela 1. As leituras foram realizadas em espectrofotômetro no comprimento de onda de 750 nm.
| Solução | Concentração molecular de Cu2+ | Transmitância % | Absorbância |
| 1 | 0,000 | -- | 0,000 |
| 2 | 0,002 | 62,95 | 0,201 |
| 3 | 0,004 | 49,77 | 0,303 |
| 4 | 0,006 | 37,93 | 0,421 |
| 5 | 0,008 | 28,11 | 0,551 |
| 6 | ? | ? | ? |
Tabela 1 – Resultados encontrados
Com os dados, foi traçado o gráfico 1.
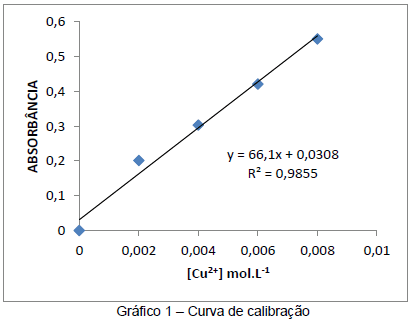
Sabendo que a absorbância da solução 6 foi de 0,245 e a transmitância 56,88, calcule a concentração da solução 6.