CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO
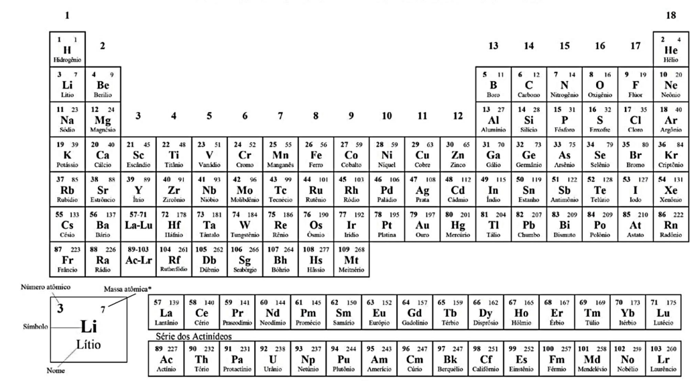
* Os valores das massas atômicas dos elementos foram arredondados para facilitar os cálculos.
Em um laboratório de química, o técnico responsável preparou 5 soluções-padrão, enumeradas de 1 a 5, e para cada uma foi registrada a concentração (mol/L) de íons OH−. Cada uma dessas soluções foi testada com dois indicadores ácido-base: índigo carmim e amarelo de alizarina. Os resultados (cores e concentração de íon hidróxido) para cada solução foram registrados na tabela a seguir:
SOLUÇÃO | [OH-] mol/L | índigo carmim | Amarelo de alizarina |
1 | 1,0×10-4 | Azul | Amarelo |
2 | 1,0×10-3 | Azul | Alaranjado |
3 | 1,0×10-2 | Azul | Vermelho |
4 | 1,0×10-1 | Verde | Vermelho |
5 | 1,0 | Amarelo | Vermelho |
Uma solução desconhecida foi entregue ao técnico para avaliar o pH dela. Sabendo que essa solução desconhecida apresentou coloração azul na presença do indicador índigo carmim e ao reagir com o indicador amarelo de alizarina apresentou coloração vermelha e, considerando as informações dispostas na tabela apresentada, pode-se afirmar que o pH dessa solução é igual a
Dados: Kw = 1,0×10−14 (25 °C); pH = − log [H+]; log 1,0 = 0; \( l \)\( o \)\( g \)(\( a \)\( b \)) = \( b \) \( l \)\( o \)\( g \) \( a \)