As propriedades físicas das substâncias, como pontos de fusão e ebulição, densidade, entre outras, podem ser explicadas pelo tipo de interação existente entre as moléculas e/ou íons. As forças que agem entre as moléculas não são tão intensas quanto as que agem em íons, mas ainda assim possibilitam que as mesmas possam existir em estados líquido e sólido. Estas forças, de natureza elétrica, podem ser de três tipos: 1- Forças do tipo dipolodipolo; 2- Forças de London e 3- Ligações de Hidrogênio. No quadro a seguir estão apresentados dados de diferentes álcoois.
|
Álcool |
Fórmula estrutural |
Massa Molar (g/mol)* |
Ponto de fusão (PF) (°C)* |
Ponto de Ebulição (PE) (°C)* |
|
Metanol |
H3C !$ - !$ OH |
32,04 |
-97,8 |
64,5 |
|
Etanol |
|
46,07 |
-114,5 |
78,3 |
|
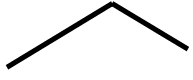
Propanol |
|
60,1 |
-127 |
96,5 - 98 |
|
Butanol |
|
74,12 |
-90 |
116 - 118 |
|
Pentanol |
|
88,15 |
-78 |
138 |
*Dados disponíveis em: https://www.sigmaaldrich.com/BR/pt. Acesso em: 26 jan. 2022.
De acordo com o quadro apresentado, verifica-se que:
 OH
OH OH
OH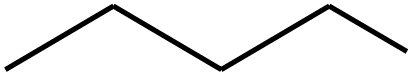 OH
OH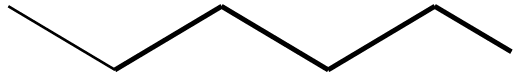 OH
OH