Foram encontradas 40 questões.
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
O conceito de solubilidade ou coeficiente de solubilidade pode ser definido como a capacidade limite de dissolução de uma determinada substância (soluto) em outra (solvente) com a qual se misture de forma homogênea. A solubilidade de uma substância está diretamente ligada à quantidade de solvente disponível e à temperatura do sistema. A curva de solubilidade de um sal hipotético pode ser apresentada como mostrado na Figura 1.
Figura 1: Curva de solubilidade de um sal hipotético em água
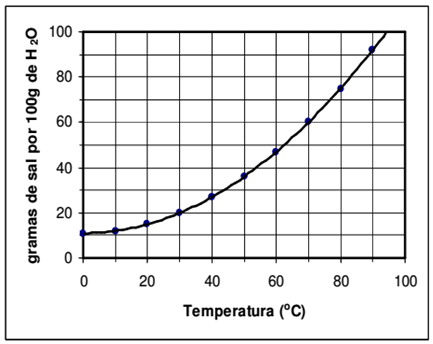
Disponível em: https://obqa.ufba.br Acesso em: 27 jan. 2022.
Considerando que, a 70°C, foram misturados 80g deste sal com 100 g de água, quando for atingido o equilíbrio
Provas
A estequiometria é a área da química que relaciona as quantidades de reagentes e produtos envolvidos em uma operação química e se baseia no princípio de que a soma das massas das substâncias reagentes em um recipiente fechado é igual à soma das massas dos produtos dessa reação.
Para se representar uma reação química, essa área utiliza equações, fórmulas, coeficientes estequiométricos adequados, além de relações intrínsecas a esse tema. Os cálculos estequiométricos podem relacionar as substâncias em quantidade de matéria (ou mol), número de partículas (moléculas, íons, átomos), massa ou volume, por exemplo.
Considere que de um determinado cilindro contendo 6,4 kg de gás metano foram removidas 18,06.1023 moléculas desse gás. Verifica se que (Dados: C = 12 g.mol-1; H = 1 g.mol-1):
Provas
"Houston, we have a problem!" Ao enviar a célebre mensagem em 13 de abril de 1970, o comandante da missão espacial Apollo 13, Jim Lovell, sabia que a sua vida e as dos seus dois companheiros estavam em risco já que um dos tanques de oxigênio (O2) da nave tinha acabado de explodir. Mesmo com o perigo iminente de os astronautas ficarem sem O2 para respirar, outra grande preocupação da NASA, a Agência Espacial responsável pela missão, era evitar que a atmosfera da espaçonave ficasse saturada com o gás carbônico (CO2) exalado pela equipe. Essa saturação poderia causar uma diminuição do pH do sangue da tripulação (chamada de acidemia sanguínea), já que o CO2 é um óxido ácido, que forma ácido carbônico quando em contato com água (CO2(g) + H2O(l) !$ arr !$ H2CO3(g)). Essa situação deveria ser evitada a qualquer custo, uma vez que ela, inicialmente, causa desorientações e desmaios, podendo evoluir até o coma ou mesmo a morte.
Normalmente, a presença de CO2 na atmosfera de uma espaçonave não é um problema. Para eliminá-lo, adaptados à ventilação, existem recipientes contendo hidróxido de lítio (LiOH), que é uma base capaz de absorver esse gás. Quimicamente falando, esse é um processo simples e lógico: remoção de um óxido ácido (CO2) da atmosfera da espaçonave através da reação com uma base (CO2(g) + 2 LiOH(s) !$ arr !$ Li2CO3(s) + H2O(l)). O problema, nesse caso, foi que os três astronautas tiveram de se refugiar numa parte da espaçonave chamada módulo lunar, que é pequena e preparada para duas pessoas. Depois de um dia e meio neste local, uma luz de alerta acendeu: o CO2 havia atingido um nível crítico, já que a quantidade de LiOH, calculada para dois astronautas, estava chegando ao final. Uma atitude improvisada, utilizando o LiOH do módulo de comando (outra área da espaçonave), salvou a vida de toda a tripulação.
PEREIRA, Luís Fernando. Química: Hidróxido de lítio salva astronautas. In: Folha de S.Paulo Folha Online Educação. São Paulo, 29 mai. 2003. Disponível em: https://www1.folha.uol.com.br/folha/educacao/ult305u12947.shtml. Acesso em: 27 jan. 2022. (Adaptado).
Uma alternativa com o mesmo efeito do LiOH seria a utilização de óxido de cálcio (CaO) para a remoção do CO2 emitido pela tripulação. De forma análoga à apresentada acima, o CaO pode reagir com o CO2 para formar o carbonato do metal alcalino terroso em questão.
Considerando os seguintes dados (C = 12 g.mol-1; Ca = 40 g.mol-1; O = 16 g.mol-1) e supondo, portanto, o uso do óxido de cálcio para a remoção do CO2 da atmosfera da espaçonave em questão, constata se que:
Provas
Por ser uma função de estado, a entalpia e, portanto, o valor de ΔH, independe do caminho entre os estados inicial e final. A variação de entalpia para um processo físico pode ser a soma das variações de dois ou mais processos separados. Do mesmo modo, a entalpia total de uma reação pode ser obtida pela soma das entalpias de reação dos passos em que a reação pode ser dividida. A entalpia da reação de hidrogenação do etino (C2H2(g) + 2 H2(g) !$ arr !$ C2H6(g)) pode ser obtida a partir da entalpia de combustão do etino -1300 kJ.mol-1, da entalpia de combustão do etano -1560 kJ.mol-1 e da entalpia de combustão do hidrogênio -286 kJ.mol-1.
Considerando as entalpias de combustão mencionadas acima, o valor para a entalpia da reação de hidrogenação do etino é:
Provas
Uma das primeiras etapas de uma análise química é a preparação da amostra a ser analisada. Tal preparação depende das características iniciais da amostra, como tamanho, pureza, umidade, dentre outras.
Amostras de sólidos de laboratório podem conter água que está em equilíbrio com a atmosfera. A presença dessas moléculas pode interferir na composição da amostra, a depender da umidade relativa do ar e da temperatura ambiente no momento da análise. Uma forma de driblar essa variabilidade na composição é a remoção da umidade dessas amostras sólidas a partir de processos de secagem, como aquecimento da amostra em estufa convencional ou a vácuo.
A água contida em sólidos pode se apresentar de duas formas: a) água essencial e b) água não essencial. Sobre esses dois tipos de “água” que podem estar presentes em sólidos, verifica se que:
Provas
Medidas invariavelmente envolvem erros e incertezas. Apenas alguns deles ocorrem devido a equívocos cometidos pelo analista. Mais comumente, os erros são causados por padronizações ou calibrações malfeitas ou variações aleatórias e incertezas nos resultados. […] No limite, entretanto, os erros envolvidos nas medidas são uma parte inerente do mundo quantitativo em que vivemos. Por conta disso, é impossível realizar uma análise química que seja totalmente livre de erros ou incertezas.
ATKINS, Peter; JONES, Loretta. Princípios de Química: questionando a vida moderna e o meio ambiente. Tradução: Ignez Caracelli et al. Bookman, 2001. (original: 1999).
Diante do exposto, é inadequado admitir que uma única análise possa fornecer informações sobre a variabilidade dos resultados. Para realizar um procedimento analítico de forma completa, os químicos costumam repetir um experimento entre duas e cincos vezes (réplicas). Uma vez que exista um conjunto de medidas para uma determinada análise, dois termos emergem como sendo relevantes na interpretação dos resultados, sendo eles:
- Precisão: é a proximidade dos resultados em relação aos demais, obtidos exatamente da mesma forma.
- Exatidão: é a proximidade de um valor medido em relação ao valor verdadeiro ou aceito.
Utilizando um jogo de dardos como modelo de experimento, tem se que o resultado ideal pode ser representado pela Figura 1, em que a maioria dos resultados atinge o centro do alvo.
Figura 1: Resultado ideal alta precisão e alta exatidão

Figura 2: Representação dos alvos A e B

Analisando os alvos A e B representados na Figura 2, verifica se que seus resultados tiveram respectivamente:
Provas
A história da Tabela Periódica pode ser comparada a uma larga avenida de duas mãos. Num primeiro sentido, foram sendo lentamente descobertos diversos elementos químicos, pelas razões e métodos os mais distintos. Depois de se conhecerem algumas dezenas de elementos, passou se a buscar correlações entre eles, para se entender suas peculiaridades, afinidades e reatividades. […] Dessa maneira se passou do conjunto de 63 elementos, conhecidos ao tempo de Mendeleev, aos 118 que constituem a Tabela Periódica moderna.
LIMA, G. M.; BARBOSA, L. C. A.; FILGUEIRAS, C. A. L. Origens e consequências da tabela periódica, a mais concisa enciclopédia criada pelo ser humano Quim. Nova, v. 42, n. 10, p. 1125 1145, 2019.
Dentre as propriedades contempladas na tabela periódica, está o raio atômico, que pode ser estimado a partir das distâncias entre os núcleos de dois átomos ligados entre si (Figura 1).
Figura 1: Esquema para a estimativa do raio atômico do átomo de cloro a partir da molécula de Cl2
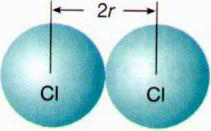
O tamanho de um determinado átomo está relacionado com o número de partículas que ele contém e também com a distribuição dos elétrons pelos seus níveis de energia. De maneira geral, a tabela periódica indica que o raio atômico de um átomo aumenta ao longo de um mesmo grupo e diminui ao longo de um mesmo período, ou seja, aumenta de cima para baixo e da direita para a esquerda (Figura 2).
Figura 2: Tendência nos valores de raios atômicos de elementos da tabela periódica
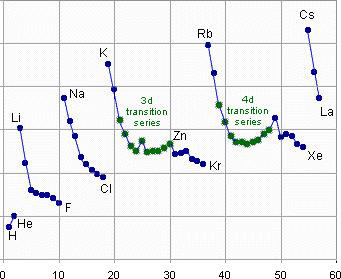
Levando se em consideração o aumento do número atômico ao longo do período, o efeito responsável por essa tendência atípica é:
Provas
A teoria dos orbitais moleculares (TOM) descreve as ligações covalentes em termos de orbitais moleculares (OM), que resultam da interação entre os orbitais atômicos (OA) dos átomos envolvidos na ligação e estão associados a moléculas como um todo. A diferença entre um orbital molecular e um orbital atômico é que este último está associado a somente um átomo.
ATKINS, Peter; JONES, Loretta. Princípios de Química: questionando a vida moderna e o meio ambiente. Tradução: Ignez Caracelli et al. Bookman, 2001. (original: 1999).
Considerando que a TOM constitui uma maneira válida de entender a formação de ligações químicas, os elétrons de valência têm uma influência na estabilidade da molécula. Assim, na formação dos orbitais moleculares a partir dos orbitais atômicos envolvidos na obtenção de uma nova molécula, verifica se que:
Provas
- SUSLei 8.080/1990: Lei Orgânica da SaúdeSistema Único de SaúdeCompetência e das AtribuiçõesArt. 15: Atribuições Comuns
Em outubro de 2020, a Associação Brasileira de Saúde Coletiva – ABRASCO, em meio ao processo pandêmico da COVID 19, publicou um importante documento com a preocupação de fortalecer o Sistema Único de Saúde (SUS). Com a colaboração de vários pesquisadores da área de Políticas, Sistemas e Serviços de saúde, elaborou uma análise sobre a atual situação e apresentou possíveis indicações para o aprimoramento do SUS. “O SUS enfrentou, desde seus primórdios, crises de financiamento e de desenvolvimento, mesmo assim se tornou a mais importante instituição de cuidado à saúde da população brasileira. Com efeito, ao longo de três décadas, o SUS logrou importantes conquistas.” (ABRASCO, 2020, p.9)
Assim, são contribuições do SUS:
Provas
- SUSLei 8.080/1990: Lei Orgânica da SaúdeSistema Único de SaúdePrincípios, Objetivos, Diretrizes e Atribuições.Art. 7º: Princípios e Diretrizes
Em um município de pequeno porte onde predominam os serviços de atenção básica (baixa densidade tecnológica), foi elaborado um programa de doenças infecciosas com foco na COVID 19. Para isso, foi considerada a realização de campanhas educativas na comunidade através de emissoras de rádio e televisão, a provisão de recursos financeiros para desenvolvimento das ações e compra de equipamentos de proteção individual, a capacitação de profissionais para atuar junto à comunidade no atendimento a pacientes com suspeita e diagnosticados com casos leves de COVID 19, o encaminhamento dos pacientes diagnosticados com casos moderado e grave de COVID 19 para níveis de média e alta de densidade tecnológica, a criação de um serviço de acompanhamento para pacientes que tiveram sequelas pós COVID 19, atendimento psicológico on-line no contexto da pandemia, entre outras atividades.
Dos princípios do SUS, apresentados no relato, ficam evidenciados os seguintes:
Provas
Caderno Container