Leia o fragmento a seguir.
A qualidade da água de consumo humano é constantemente monitorada, e a determinação do teor de cloreto é uma etapa fundamental desse controle. Além do método de Mohr, outra estratégia clássica é o método de Volhard, no qual se adiciona excesso conhecido de solução padrão de nitrato de prata (AgNO₃) à amostra contendo íons cloreto. Após a formação completa do precipitado de cloreto de prata (AgCl), o excesso de prata em solução é titulado com solução padrão de tiocianato de potássio (KSCN), utilizando íons férricos (Fe³⁺) como indicador.
(Adaptado de VOGEL, Arthur I. Análise Química Quantitativa. Rio de Janeiro: LTC, 2020.)
Uma amostra de 25,0 mL de água de rio foi analisada pelo método de Volhard. Inicialmente, adicionou-se 30,0 mL de solução de AgNO₃ 0,0200 mol·L⁻¹ e após a precipitação de todo o Cl⁻ como AgCl, o excesso de Ag⁺ foi titulado com 8,0 mL de solução de KSCN 0,0150 mol·L⁻¹.
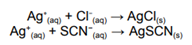
e as massas molares aproximadas: Ag = 108 g/mol, Cl = 35,5 g/mol, C = 12 g/mol, S = 32 g/mol e N = 14g/mol. A concentração de cloreto em mg·L⁻¹ na amostra é
Considerando as reações:
A qualidade da água de consumo humano é constantemente monitorada, e a determinação do teor de cloreto é uma etapa fundamental desse controle. Além do método de Mohr, outra estratégia clássica é o método de Volhard, no qual se adiciona excesso conhecido de solução padrão de nitrato de prata (AgNO₃) à amostra contendo íons cloreto. Após a formação completa do precipitado de cloreto de prata (AgCl), o excesso de prata em solução é titulado com solução padrão de tiocianato de potássio (KSCN), utilizando íons férricos (Fe³⁺) como indicador.
(Adaptado de VOGEL, Arthur I. Análise Química Quantitativa. Rio de Janeiro: LTC, 2020.)
Uma amostra de 25,0 mL de água de rio foi analisada pelo método de Volhard. Inicialmente, adicionou-se 30,0 mL de solução de AgNO₃ 0,0200 mol·L⁻¹ e após a precipitação de todo o Cl⁻ como AgCl, o excesso de Ag⁺ foi titulado com 8,0 mL de solução de KSCN 0,0150 mol·L⁻¹.
e as massas molares aproximadas: Ag = 108 g/mol, Cl = 35,5 g/mol, C = 12 g/mol, S = 32 g/mol e N = 14g/mol. A concentração de cloreto em mg·L⁻¹ na amostra é
Considerando as reações: