Foram encontradas 50 questões.
Um laboratório analisou o extrato aquoso de um solo contaminado, próximo a um lixão, onde foram
descartadas pilhas usadas. Na aplicação da marcha analítica de cátions, observou-se o seguinte:
1. Adição de HCl diluído: formou-se precipitado branco parcialmente solúvel em água quente.
2. Filtrado acidificado + H₂S (meio ácido): formou-se precipitado amarelo.
3. Novo filtrado + NH₄Cl/NH₄OH: não houve precipitado. Em seguida, com a solução amoniacal, borbulhou-se H₂S e formou-se precipitado preto.
De acordo com o exposto, são identificados, respectivamente, em (1), (2) e (3),
1. Adição de HCl diluído: formou-se precipitado branco parcialmente solúvel em água quente.
2. Filtrado acidificado + H₂S (meio ácido): formou-se precipitado amarelo.
3. Novo filtrado + NH₄Cl/NH₄OH: não houve precipitado. Em seguida, com a solução amoniacal, borbulhou-se H₂S e formou-se precipitado preto.
De acordo com o exposto, são identificados, respectivamente, em (1), (2) e (3),
Provas
Questão presente nas seguintes provas
Em um laboratório de análise de conformidade, utilizou-se a cromatografia gasosa (GC) para analisar resíduos
de pesticidas em frutas. Dois compostos, A e B, apresentaram massas molares semelhantes e pontos de
ebulição próximos, resultando em picos sobrepostos no cromatograma inicialmente obtido.
Considerando o princípio da GC e os fatores que influenciam a separação cromatográfica, para melhorar o resultado obtido ampliando a separação entre os picos, o analista deve considerar
Considerando o princípio da GC e os fatores que influenciam a separação cromatográfica, para melhorar o resultado obtido ampliando a separação entre os picos, o analista deve considerar
Provas
Questão presente nas seguintes provas
Leia o fragmento a seguir.
O dióxido de enxofre (SO2) e seus sais são adicionados à vinificação desde o século XVII. O SO2 e seus sais de sulfito continuam sendo um aditivo essencial na vinificação, visto que não há nenhum outro aditivo com as mesmas propriedades duplas de antioxidante e preservação. Em quantidades superiores a 10 mg/L, ele continua sendo um produto potencialmente tóxico e causador de reações adversas para consumidores e vinicultores, devendo, portanto, ser manuseado com cuidado. Além disso, os sulfitos também são usados como agentes biocidas na desinfecção de barris.
(Adaptado de OIV – International Organisation of Vine and Wine, 2021)
Em uma análise laboratorial, 50,0 mL de vinho foram tratados para liberar todo o SO₂, que foi em seguida absorvido em excesso de solução padrão e posteriormente titulado com NaOH 0,0100 mol·L⁻¹. O volume de base consumido até o ponto de viragem da fenolftaleína foi de 12,5 mL. Considerando as equações simplificadas:
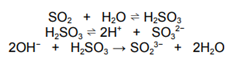
e sabendo que a massa molar de SO₂ = 64 g/mol, a concentração de SO₂ na amostra de vinho em mg/L é de
O dióxido de enxofre (SO2) e seus sais são adicionados à vinificação desde o século XVII. O SO2 e seus sais de sulfito continuam sendo um aditivo essencial na vinificação, visto que não há nenhum outro aditivo com as mesmas propriedades duplas de antioxidante e preservação. Em quantidades superiores a 10 mg/L, ele continua sendo um produto potencialmente tóxico e causador de reações adversas para consumidores e vinicultores, devendo, portanto, ser manuseado com cuidado. Além disso, os sulfitos também são usados como agentes biocidas na desinfecção de barris.
(Adaptado de OIV – International Organisation of Vine and Wine, 2021)
Em uma análise laboratorial, 50,0 mL de vinho foram tratados para liberar todo o SO₂, que foi em seguida absorvido em excesso de solução padrão e posteriormente titulado com NaOH 0,0100 mol·L⁻¹. O volume de base consumido até o ponto de viragem da fenolftaleína foi de 12,5 mL. Considerando as equações simplificadas:
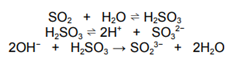
e sabendo que a massa molar de SO₂ = 64 g/mol, a concentração de SO₂ na amostra de vinho em mg/L é de
Provas
Questão presente nas seguintes provas
Leia o fragmento a seguir.
A qualidade da água de consumo humano é constantemente monitorada, e a determinação do teor de cloreto é uma etapa fundamental desse controle. Além do método de Mohr, outra estratégia clássica é o método de Volhard, no qual se adiciona excesso conhecido de solução padrão de nitrato de prata (AgNO₃) à amostra contendo íons cloreto. Após a formação completa do precipitado de cloreto de prata (AgCl), o excesso de prata em solução é titulado com solução padrão de tiocianato de potássio (KSCN), utilizando íons férricos (Fe³⁺) como indicador.
(Adaptado de VOGEL, Arthur I. Análise Química Quantitativa. Rio de Janeiro: LTC, 2020.)
Uma amostra de 25,0 mL de água de rio foi analisada pelo método de Volhard. Inicialmente, adicionou-se 30,0 mL de solução de AgNO₃ 0,0200 mol·L⁻¹ e após a precipitação de todo o Cl⁻ como AgCl, o excesso de Ag⁺ foi titulado com 8,0 mL de solução de KSCN 0,0150 mol·L⁻¹.
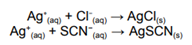
e as massas molares aproximadas: Ag = 108 g/mol, Cl = 35,5 g/mol, C = 12 g/mol, S = 32 g/mol e N = 14g/mol. A concentração de cloreto em mg·L⁻¹ na amostra é
Considerando as reações:
A qualidade da água de consumo humano é constantemente monitorada, e a determinação do teor de cloreto é uma etapa fundamental desse controle. Além do método de Mohr, outra estratégia clássica é o método de Volhard, no qual se adiciona excesso conhecido de solução padrão de nitrato de prata (AgNO₃) à amostra contendo íons cloreto. Após a formação completa do precipitado de cloreto de prata (AgCl), o excesso de prata em solução é titulado com solução padrão de tiocianato de potássio (KSCN), utilizando íons férricos (Fe³⁺) como indicador.
(Adaptado de VOGEL, Arthur I. Análise Química Quantitativa. Rio de Janeiro: LTC, 2020.)
Uma amostra de 25,0 mL de água de rio foi analisada pelo método de Volhard. Inicialmente, adicionou-se 30,0 mL de solução de AgNO₃ 0,0200 mol·L⁻¹ e após a precipitação de todo o Cl⁻ como AgCl, o excesso de Ag⁺ foi titulado com 8,0 mL de solução de KSCN 0,0150 mol·L⁻¹.
e as massas molares aproximadas: Ag = 108 g/mol, Cl = 35,5 g/mol, C = 12 g/mol, S = 32 g/mol e N = 14g/mol. A concentração de cloreto em mg·L⁻¹ na amostra é
Considerando as reações:
Provas
Questão presente nas seguintes provas
Na fase de purificação de um determinado composto orgânico obtido por síntese química, foi escolhida a
cristalização fracionada como método de separação. Sobre esse procedimento, é correto afirmar que
Provas
Questão presente nas seguintes provas
Em uma disciplina de Análise Química, os estudantes realizaram simulações virtuais de uma titulação
ácido-base. Durante a prática, observaram que o ponto de viragem indicado pelo software coincidia
exatamente com o ponto de equivalência teórico, sem apresentar variações. Quando a mesma titulação foi
realizada em um laboratório real, as titulações mostraram valores de volume gasto no ponto final ligeiramente
diferentes, mesmo entre grupos que usaram o mesmo ácido e a mesma base padronizada.
A discrepância entre o ambiente simulado e o ambiente real, pode ser explicada pelo fato de que,
A discrepância entre o ambiente simulado e o ambiente real, pode ser explicada pelo fato de que,
Provas
Questão presente nas seguintes provas
Um laboratorista que trabalha no controle de qualidade de uma indústria de bebidas, utiliza a
espectrofotometria UV-Vís, para determinar o teor de corante em bebidas artificiais. Considerando o princípio
da Lei de Lambert - Beer e suas limitações, assinale a opção correta.
Provas
Questão presente nas seguintes provas
Leia o fragmento a seguir.
A Espectrometria de Absorção Atômica (AAS) é uma técnica instrumental amplamente utilizada para determinar metais em baixas concentrações em amostras ambientais, alimentícias e biológicas. O princípio básico consiste em atomizar os elementos presentes na amostra — geralmente em uma chama ou em um forno de grafite — e medir a absorção de radiação emitida por uma lâmpada específica para o elemento de interesse. Como cada átomo possui níveis de energia eletrônica bem definidos, a absorção de luz em determinado comprimento de onda é característica de cada elemento químico, permitindo tanto a identificação quanto a quantificação.
(Adaptado de HARRIS,Daniel C. Análise Química Quantitativa. Rio de Janeiro: LTC, 2020)
A técnica de Absorção Atômica é frequentemente aplicada em análises de metais pesados em alimentos e águas. Sobre o princípio de funcionamento da Espectrometria de Absorção Atômica, é correto afirmarmos que,
A Espectrometria de Absorção Atômica (AAS) é uma técnica instrumental amplamente utilizada para determinar metais em baixas concentrações em amostras ambientais, alimentícias e biológicas. O princípio básico consiste em atomizar os elementos presentes na amostra — geralmente em uma chama ou em um forno de grafite — e medir a absorção de radiação emitida por uma lâmpada específica para o elemento de interesse. Como cada átomo possui níveis de energia eletrônica bem definidos, a absorção de luz em determinado comprimento de onda é característica de cada elemento químico, permitindo tanto a identificação quanto a quantificação.
(Adaptado de HARRIS,Daniel C. Análise Química Quantitativa. Rio de Janeiro: LTC, 2020)
A técnica de Absorção Atômica é frequentemente aplicada em análises de metais pesados em alimentos e águas. Sobre o princípio de funcionamento da Espectrometria de Absorção Atômica, é correto afirmarmos que,
Provas
Questão presente nas seguintes provas
Em uma aula de Análise Química, um estudante realizou a determinação gravimétrica do teor de cloreto (Cl
-
)
em uma amostra de água de uma lagoa. Para isso, diluiu a amostra em água destilada, isenta de cloretos, e
adicionou excesso de solução de nitrato de prata (AgNO3
), formando um precipitado branco de cloreto de prata
(AgCl), insolúvel em meio aquoso:
Ag⁺(aq) + Cl⁻(aq) → AgCl(s)
Após filtração, lavagem, secagem e pesagem, obteve-se 0,286 g de AgCl. Considerando as massa molares aproximadas: Ag = 108 g/mol; Cl = 35,5 g/mol; a massa de cloreto (Cl-) presente na amostra original é de
Ag⁺(aq) + Cl⁻(aq) → AgCl(s)
Após filtração, lavagem, secagem e pesagem, obteve-se 0,286 g de AgCl. Considerando as massa molares aproximadas: Ag = 108 g/mol; Cl = 35,5 g/mol; a massa de cloreto (Cl-) presente na amostra original é de
Provas
Questão presente nas seguintes provas
Leia o fragmento a seguir.
A contaminação por mercúrio em rios da Amazônia, decorrente do garimpo ilegal, é uma ameaça crescente à biodiversidade e à saúde das populações ribeirinhas. Uma das formas de identificar a presença desse metal em amostras ambientais é recorrer a métodos analíticos clássicos de análise sistemática de cátions, empregados historicamente em laboratórios para caracterização de íons metálicos em solução.
(Adaptado de reportagem – Agência Brasil, 2024)
Na análise sistemática de cátions, os íons metálicos são separados em grupos, de acordo com a formação de precipitados característicos, frente a reagentes específicos. O íon Hg²⁺ (mercúrio II) pertence ao primeiro grupo de cátions.
Considere uma amostra de água coletada em área de garimpo ilegal, suspeita de contaminação por mercúrio. Para caracterizar a presença de Hg²⁺, utilizando a análise sistemática, deve-se adicionar à amostra uma solução de
A contaminação por mercúrio em rios da Amazônia, decorrente do garimpo ilegal, é uma ameaça crescente à biodiversidade e à saúde das populações ribeirinhas. Uma das formas de identificar a presença desse metal em amostras ambientais é recorrer a métodos analíticos clássicos de análise sistemática de cátions, empregados historicamente em laboratórios para caracterização de íons metálicos em solução.
(Adaptado de reportagem – Agência Brasil, 2024)
Na análise sistemática de cátions, os íons metálicos são separados em grupos, de acordo com a formação de precipitados característicos, frente a reagentes específicos. O íon Hg²⁺ (mercúrio II) pertence ao primeiro grupo de cátions.
Considere uma amostra de água coletada em área de garimpo ilegal, suspeita de contaminação por mercúrio. Para caracterizar a presença de Hg²⁺, utilizando a análise sistemática, deve-se adicionar à amostra uma solução de
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container