Uma quantidade de \( n \) moles de um gás ideal realiza um processo do estado inicial \( i \) para o estado final \( f \), conforme mostrado no diagrama \( P \) − \( V \) abaixo. As quantidades \( P \)0 e \( V \)0 representam os valores extrapolados da reta sobre os eixos pressão e volume, respectivamente. Considere \( R \) a constante universal dos gases ideais. Com base nos dados apresentados, analise as assertivas abaixo:
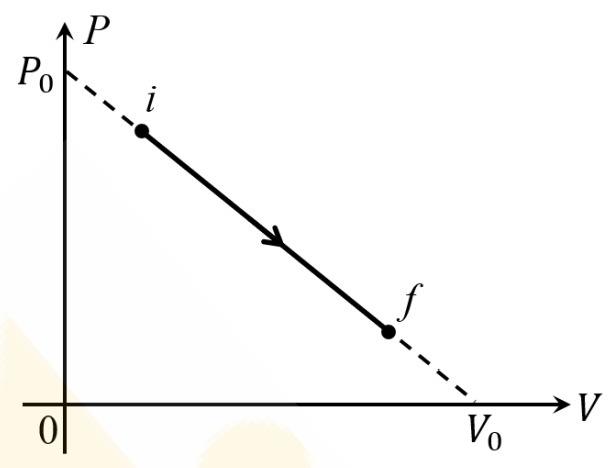
I. A pressão e o volume do gás em qualquer estado ao longo da transformação \( i \) → \( f \) satisfazem a relação \( P \)\( V \) = \( P \)0\( V \)0.
II. A temperatura do gás no processo \( i \) → \( f \) varia com o volume do gás de acordo com a expressão \( T \) = \( \dfrac{P_0V_0}{nR}\left(\dfrac{V}{V_0}\right)\left(1-\dfrac{V}{V_0}\right). \)
III. Considerando que o volume do gás começa muito próximo de zero (\( V \) → 0) e aumenta monotonamente até \( V \)0, a temperatura máxima possível que o gás pode atingir nesse processo é \( T \)máx = \( \dfrac{P_0V_0}{nR}. \)
Quais estão corretas?