A figura a seguir representa uma pilha eletroquímica de cobre e prata (Pilha Ag/Cu), composta por dois
eletrodos imersos em soluções de seus respectivos íons na concentração de 1,0 mol/L, conectados por um
voltímetro e uma ponte salina. Este arranjo permite a conversão de energia química em energia elétrica por
meio de reações de oxirredução espontâneas.
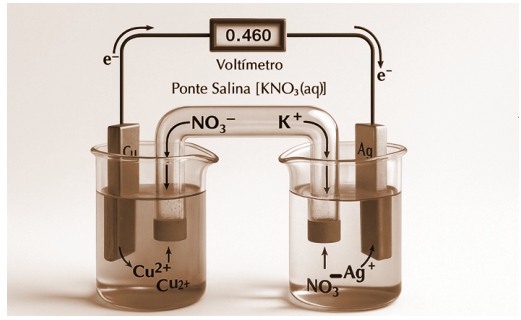
Representação esquemática de uma pilha Cu–Ag (adaptado de Eletroquímica, Instituto de Química – USP, p. 34, disponível em: https://www.iq.usp.br/fmvichi/html/Eletroquimica.pdf, acesso em: 21 ago. 2025. Baseado em Pearson Prentice Hall, 2007).
Com base na análise da Pilha Ag/Cu apresentada na figura e nos princípios da eletroquímica, assinale a opção que apresenta a afirmação correta.

Representação esquemática de uma pilha Cu–Ag (adaptado de Eletroquímica, Instituto de Química – USP, p. 34, disponível em: https://www.iq.usp.br/fmvichi/html/Eletroquimica.pdf, acesso em: 21 ago. 2025. Baseado em Pearson Prentice Hall, 2007).
Com base na análise da Pilha Ag/Cu apresentada na figura e nos princípios da eletroquímica, assinale a opção que apresenta a afirmação correta.