Foram encontradas 40 questões.
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Em um laboratório de química, um técnico utilizou as substâncias HC\( \ell \), NaOH e NaC\( \ell \) para preparar soluções aquosas 0,01 mol L-1 de cada uma e NH4C\( \ell \) para preparar uma solução aquosa 5% m/v. Em todas as soluções foi utilizada água destilada tratada para remoção do CO2 dissolvido. Contudo, após o preparo, o técnico se esqueceu de identificar os quatro balões volumétricos que continham as soluções incolores em questão. Na tentativa de identificar as soluções, ele numerou os balões volumétricos de 1 a 4, retirou alíquotas de cada solução e fez testes com os indicadores: azul de bromotimol, alaranjado de metila e fenolftaleína (soluções indicadoras preparadas previamente).
O técnico obteve os resultados presentes no Quadro abaixo ao realizar os testes.
|
Soluções |
Cor da solução na presença azul de bromotimol | Cor da solução na presença de alaranjado de metila |
Cor da solução na presença de fenolftaleína |
| 1 | amarela | vermelha | - |
| 2 | azul | amarela | - |
| 3 | amarela | amarela |
incolor |
| 4 | verde | - |
incolor |
De acordo com os resultados, o técnico concluiu que as soluções 1, 2 , 3 e 4 eram, respectivamente,
|
Dados cores dos indicadores em diferentes faixas de pH (valores aproximados). |
||
|
Azul de bromotimol |
Alaranjado de metila |
Fenolftaleína |
|
pH < 6,0 – cor amarela |
pH \( \le \) 3,1 – cor vermelha |
pH < 8,2 – incolor |
|
pH entre 6,0 e 7,6 – cor verde |
pH entre 3,2 e 4,4 – cor laranja |
pH entre 8,2 e 10,0 – cor rosa claro |
|
pH > 7,6 – cor azul |
pH > 4,4 cor amarela |
pH > 10 cor rosa intenso |
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Esse processo é conhecido como
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
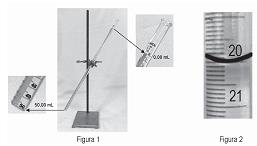
Acrescentou água até a marcação indicada na Figura 2, fez a leitura para chegar ao volume contido e constatou que o valor do erro relativo percentual na medida do volume contido, levando em conta a leitura a partir do menisco inferior, é, aproximadamente,
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química CinéticaTransformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A massa, em gramas, de PbI 2 , sólido que se forma ao se misturarem 100,00 mL de cada uma das soluções, é
Dados M(KI) = 166 g/mol M(Pb(NO3)2) = 331 g/mol M(Pbl2) = 461 g/mol
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
KHC8 H4 O4(aq) + NaOH(aq) → KNaC8 H4 O4(aq) + H2 O(l)
A solução aquosa de NaOH a ser padronizada e a água usada na preparação do padrão primário foram tratadas para ficar isentas de CO2 dissolvido. Em pesa-filtro de forma baixa pesaram-se 7,4245 g de biftalato de potássio. A essa massa foi adicionada água suficiente para a sua dissolução total de forma que o padrão primário fosse transferido quantitativamente para balão volumétrico de 250,00 mL, onde o volume foi ajustado até o traço de referência pela adição de água. Uma alíquota de 25,00 mL dessa solução foi titulada com a solução de NaOH, usando a fenolftaleína como indicador do ponto final.
Sendo o volume da solução aquosa de NaOH gasto na titulação, até a mudança de cor da fenolftaleína para rosa claro, igual a 22,78 mL, a concentração em quantidade de matéria (mol/L) da solução de NaOH é
Dado M(KHC8H4O4) = 204,23 g/mol
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
1º ) Transfira uma solução padrão de permanganato de potássio 0,5000 mol/L para uma bureta limpa e seca.
2º ) Pipete 25,00 mL de amostra de água oxigenada comercial para um balão volumétrico de 250,00 mL, acrescente água destilada até o traço de referência e faça a homogeneização. Dessa solução, pipete uma alíquota de 25,00 mL para um frasco Erlenmeyer, acrescente ±100 mL de água destilada e 5 mL de ácido sulfúrico concentrado.
3º ) Titule o H2 O2 contido na alíquota com a solução padrão de permanganato de potássio até coloração levemente violeta (1º excesso de KMnO4 ).
A reação que ocorre na titulação é:
2 MnO4 - (aq) + 5 H2 O2(aq) + 6 H+ (aq) → 2 Mn2+ (aq) + 5 O2(g) + 8 H2 O(l)
Seguindo esse roteiro, o volume de solução de permanganato de potássio gasto na titulação da alíquota no frasco Erlenmeyer foi igual a 30,40 mL.
Com base nos resultados da análise, o técnico constatou que a porcentagem massa por volume (g H2 O2 /100 mL água oxigenada) na amostra original é igual a
Dado M(H2O2) = 34,00 g/mol
Provas
HC2 H3 O2(aq) + H2 O(l)
Com o objetivo de estudar a variação do valor do pH (capacidade freadora ou de tamponamento) dessa solução, um técnico fez experiências adicionando a três alíquotas da solução um volume específico das seguintes substâncias: (i) água pura, (ii) uma solução aquosa de base forte e (iii) uma solução aquosa de ácido forte.
Considerando esse equilíbrio e as condições externas que podem perturbá-lo até que se atinja um novo equilíbrio, constata-se que na adição de 10,0 mL de
Provas

Observe as afirmações a seguir relativas à preparação de soluções e aos cuidados com o uso de balões volumétricos.
I - A incerteza relativa de um balão volumétrico classe A diminui com o aumento do volume do mesmo.
II - O erro de paralaxe no ajuste de volume é causado pelas variações de temperatura que afetam o coeficiente de dilatação do vidro.
III - Um balão volumétrico pode ser resfriado previamente na geladeira para aumentar a estabilidade da solução preparada.
Está correto o que se afirma em:
Provas
Provas
Os resultados (cinco réplicas) obtidos a partir de uma determinação da concentração de um analito em uma amostra são mostrados na Tabela abaixo.
|
Réplica |
1 | 2 | 3 | 4 | 5 |
|
Resultado (em \( \mu \)g . g-1) |
10,5 | 10,4 | 10,5 | 10,5 | 10,6 |
Se o resultado verdadeiro para o analito na amostra é 10,0 \( \mu \)g . g-1, é possível concluir que o(a)
Provas
Caderno Container