Foram encontradas 50 questões.
Nos itens I, II, III e IV, descrevem-se procedimentos analíticos qualitativos para evidenciar a presença de ânions.
I. Adição de ácido sulfúrico concentrado a uma amostra em solução aquosa resulta na formação de um anel marrom se brometo, iodeto e nitrito estiverem ausentes.
II. A ação do ácido sulfúrico sobre uma amostra sólida seguida da coleta do produto reacional sobre água de barita resulta em turvação da solução.
III. A adição de ácido sulfúrico concentrado a uma amostra sólida seguida da adição de álcool isoamílico resulta em produto com odor característico.
IV. A adição de solução de cloreto de cálcio sobre amostra em solução aquosa resulta em formação imediata de precipitado branco.
Os testes descritos nos itens I, II, III e IV são confirmatórios, respectivamente, para os íons
Provas
A batraquiotoxina é uma substância natural altamente tóxica produzida por rãs encontradas na floresta amazônica. Ela tem fórmula molecular C31H42N2O6
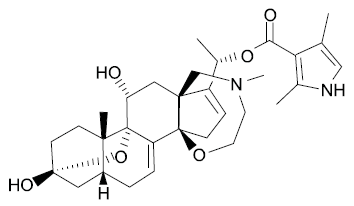
Na molécula da batraquiotoxina, são encontradas as funções orgânicas
Provas
Os catalisadores automotivos aceleram a conversão dos poluentes gases veiculares em compostos menos prejudiciais ao meio ambiente. Para uma reação do tipo !$ A+B \leftrightarrow C+D !$ apresenta-se uma curva variação de energia em função do caminho de reação com o catalisador e sem o catalisador.
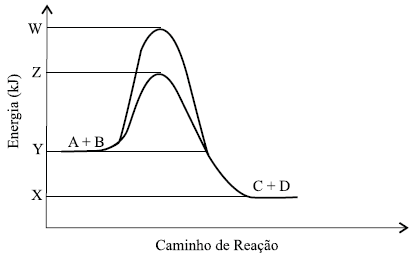
Em relação à ação do catalisador, nesse processo afirma-se que
I. o catalisador aumenta a velocidade das reações direta e inversa;
II. a diminuição da energia de ativação é a mesma para as reações direta e inversa;
III. o catalisador desloca o equilíbrio da reação no sentido da formação dos produtos.
É correto o que se afirma em
Provas
Um experimento cinético envolvendo a reação !$ A+2B\rightarrow 2D !$ perimento, monitorou-se a velocidade da reação em uma dada temperatura. Mantendo-se a mesma temperatura, duplicou-se a concentração inicial do reagente A mantendo-se a mesma concentração do reagente B e verificou-se que a velocidade da reação foi o dobro da primeira. No terceiro experimento, mantiveram-se as condições de temperatura e concentração do reagente A iguais às do primeiro experimento e duplicou-se a concentração do reagente B. Verificou-se que a velocidade da reação foi a mesma do primeiro experimento. Com base nos resultados experimentais, é correto afirmar que a ordem global dessa reação é igual a
Provas
Se um uma solução aquosa, levemente ácida a 20oC , contendo íons Ba2+ e Sr2+, for gotejada, lenta e continuamente sob agitação, uma solução diluída de sulfato de sódio, é correto afirmar
que Produtos de solubilidade a 20 ºC
Ks (SrSO4) = 3 x 10-7
Ks(BaSO4) = 9 x 10-11
Provas
Uma substância altamente tóxica fabricada em larga escala como solvente tem em sua composição apenas carbono, hidrogênio e oxigênio. A análise elementar por combustão de 12,6 mg dessa substância resultou em 26,4 mg de dióxido de carbono e 5,4 mg de água.
A fórmula mínima dessa substância é
Provas
Sobre dois líquidos com fórmula molecular C4H10O, o éter dietílico e o álcool isobutílico, são feitas as seguintes afirmações:
I. durante a ebulição desses dois líquidos, num mesmo local, a pressão de vapor do éter dietílico será mais alta que a pressão de vapor do álcool isobutílico;
II. o éter dietílico tem ponto de ebulição mais baixo que o álcool isobutílico;
III. a viscosidade do éter dietílico é mais alta que a do álcool isobutílico;
IV. a entralpia de vaporização molar !$ \Delta Hº_{vap} !$, do álcool isobutílico é mais alta do que a do éter dietílico.
É correto apenas o que se afirma em
Provas
As baterias de prata, representadas pelo diagrama
Zn(s) | ZnO(s) | KOH(aq) | Ag2O(s)| Ag(s)
são empregadas em equipamentos como câmeras fotográficas e dispositivos médicos como marcapassos e implantes auditivos.
Em relação a essa bateria é correto afirmar que durante seu funcionamento forma-se
Provas
O óxido de nitrogênio, NO, é uma substância que desempenha no organismo humano atividade essencial quando em pequenas quantidades, atuando como neurotransmissor e vasodilatador. Entretanto, ao ser produzido nos processos de combustão nos motores de automóveis e aviões, este óxido é um poluente atmosférico.
Em pequena escala laboratorial, o NO pode ser obtido pela reação do íon nitrito, NO2 -, e íon iodeto, I-, em meio aquoso ácido, formando-se também como subproduto o iodo, I2.
O somatório dos menores valores inteiros dos coeficientes estequiométricos da equação iônica do processo laboratorial de obtenção do NO é igual a
Provas
Considerando-se a tabela com dados dos átomos dos elementos representados pelos símbolos X, M e J
|
Elemento |
Prótons |
Nêutrons |
| X | 20 | 20 |
| M | 20 | 22 |
| J | 19 | 20 |
são feitas as seguintes afirmações:
I. a espécie X2+ tem raio maior do que o raio do átomo X;
II. X e M são isóbaros;
III. X e J são isótonos;
IV. as espécies X2+ e J+ são isoeletrônicas.
É correto o que se afirma apenas em
Provas
Caderno Container