Foram encontradas 50 questões.
A base da análise gravimétrica é a pesagem de uma substância obtida pela precipitação de uma solução. Após a obtenção e filtração, o precipitado precisa ser secado antes da pesagem.
O precipitado pode conter água de várias formas:
I. presente na superfície, sua quantidade depende da umidade da atmosfera;
II. presente em soluções sólidas ou em cavidades nos cristais;
III. associada a substância com grande superfície interna, como óxidos hidratados;
IV. presente como água de hidratação, ou de cristalização.
As diferentes formas de apresentação de água nos sólidos obtidos na precipitação descritas como I, II, II e IV são, correta e respectivamente, denominadas água
Provas
Uma importante técnica de separação usada em química analítica envolve o uso de colunas de troca iônica.
O termo troca iônica refere-se à troca de íons de cargas com . Na preparação adequada do procedimento de troca iônica emprega-se uma coluna de vidro (bureta) na qual se acomoda o material trocador de íons. Esse deve ser na solução empregada na eluição da coluna.
Um exemplo de aplicação dessa técnica consiste na separação dos cátions Co2+e Ni2+ de uma mistura em solução aquosa. Como apenas o cátion Co2+ forma espécie complexa negativa com ânion cloreto, sua separação da mistura por retenção pode ser feita usando-se uma coluna repleta de uma resina trocadora .
Assinale a alternativa que completa, correta e respectivamente, as lacunas do texto.
Provas
As pipetas são instrumentos de vidro empregadas em medidas precisas na transferência de líquido. A sucção do líquido para o interior da pipeta é feita usando-se pipetadores, dos quais o mais usual é a pera de borracha.
Na etapa de liberação do líquido medido na pipeta, é importante observar se o líquido retido na extremidade interna inferior da pipeta deve ou não ser forçado para fora da pipeta. Antigamente, quando indicada, essa operação era feita soprando-se a pipeta; atualmente ela é feita, usando-se a pera de borracha.
Nas figuras, apresentam-se dois tipos de identificação em pipetas e um pipetador tipo pera de borracha.
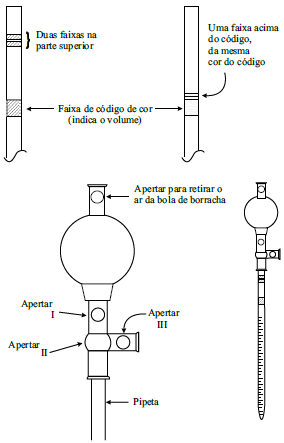
(Constantino, M.G, Silva, G.V.J., Donate, P. M. Fundamentos de Química Experimental, 2. ed, Edusp, 2011.)
O número de faixas de demarcação na pipeta em que deve ser feita a expulsão (sopragem) completa do líquido e o local da pera de borracha que deve ser apertado para soprar o líquido retido no final da pipetagem são, respectivamente,
Provas
Um ensaio qualitativo para identificação de um ânion emprega a aparelhagem da figura.
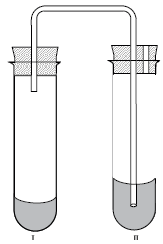
No tubo I é adicionada a amostra sólida, solução de ácido clorídrico, e o tubo é fechado imediatamente com a rolha. A conexão de vidro em U deve estar previamente montada, imersa em uma solução aquosa de hidróxido de bário no tubo II. A turvação da solução do tubo II evidencia que na amostra existe o ânion
Provas
Na identificação de cátions em análises qualitativas, empregam- se etapas envolvendo reações com bases fracas e com bases fortes.
Alguns cátions metálicos formam espécies complexas solúveis em água dos tipo
I – [M(NH3)x]a+
II – [M(OH)x]b–
onde M corresponde ao cátion metálico.
Ocorre a formação tanto da espécie I na reação com excesso de base fraca, como da espécie II em reação com excesso de base forte quando o cátion metálico M analisado é
Provas
Um composto isolado do leite de vaca apresenta, na sua composição, apenas carbono, oxigênio e hidrogênio. A análise por combustão de um milimol desse composto gerou quatro milimols de CO2 e quatro milimols de H2O. Os resultados da análise instrumental de CHN mostram que o teor percentual de hidrogênio em massa nesse composto corresponde a ¼ do valor do teor percentual em massa de oxigênio.
A fórmula mínima desse composto é
Provas
Pesquisa realizada em dosagem de contaminantes em esgoto doméstico revelou a presença de hormônios e antibióticos decorrentes de urina e fezes de indivíduos que fazem uso dessa medicação.
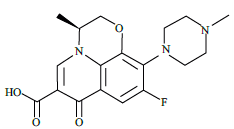
Na molécula de levofloxacin, são encontrados grupos funcionais característicos de
Provas
Um estudo cinético envolvendo a reação
2 A + B + C !$ \rightarrow !$ 2D + E
foi realizado com três experimentos de medida de velocidade de reação sob a mesma temperatura e condições de agitação.
|
Experimento |
A mol L–1 |
B mol L–1 |
C mol L–1 |
Velocidade |
| 1 | 0,1 | 0,1 | 0,1 | 3,0 x 10-4 |
| 2 | 0,05 | 0,1 | 0,1 | 3,0 x 10-4 |
| 3 | 0,05 | 0,3 | 0,1 | 9,0 x 10-4 |
Sabe-se que a reação tem ordem global igual a quatro. Com base nos resultados experimentais, é correto afirmar que os valores de ordem de reação para o consumo das substâncias A, B e C são, respectivamente,
Provas
O estanho é usado no revestimento de embalagens metálicas de alimentos. Sua obtenção pode ser feita por processo eletrolítico em soluções aquosas contendo cloreto de estanho (II).
A reação global do processo eletrolítico é Sn2+(aq) + 2 Cl–(aq) !$ \rightarrow !$ Sn (s) + Cl2 (g)
Dados:
Cl2 (g) + 2e– !$ \rightarrow !$ 2 Cl– (aq) Eº = + 1,36 V
Sn2+ (aq) + 2e– !$ \rightarrow !$ Sn (s) Eº = – 0,14 V
É correto afirmar que, na eletrólise de uma solução aquosa 1,0 mol. L–1 de cloreto de estanho (II) a 25 ºC, o produto formado no catodo, o potencial teórico aplicado e a polaridade do anodo são, respectivamente,
Provas
A determinação de monóxido de carbono em amostras gasosas pode ser feita por meio da passagem da mistura gasosa contendo CO por um absorvedor sólido aquecido a 150 ºC contendo I2O5. Forma-se iodo elementar e dióxido de carbono (reação I). O iodo é destilado e absorvido em uma solução aquosa de tiossulfato de sódio com concentração conhecida.
I2(g) + 2 S2O3 2–(aq) !$ \rightarrow !$ 2I–(aq) + S4O6 2–(aq) (reação II)
O excesso de tiossulfato é retrotitulado e, dessa forma, a quantidade de monóxido de carbono é indiretamente determinada.
A soma dos menores valores inteiros dos coeficientes estequiométricos da equação de reação I e o agente oxidante da reação II são, respectivamente,
Provas
Caderno Container