Foram encontradas 30 questões.
O gráfico abaixo representa o termograma obtido na análise termogravimétrica do CuSO4.5H2O, aquecido a 10 ºC/min, na presença de ar, em cadinho de platina. A primeira perda de massa se dá entre 90 ºC e 150 ºC (região A), a segunda ocorre entre 200 ºC e 275 ºC (região B), a terceira decomposição, entre 700 ºC e 900 oC (região C) e a última ocorre entre 1000 ºC e 1100ºC (região D). (Dados: Massas molares: CuSO4.5H2O = 249,5 g/mol; H2O = 18 g/mol; CuO = 79,5 g/mol; Cu = 63,5 g/mol)
A respeito dos fenômenos que ocorrem nas regiões citadas, é correto afirmar que:
Provas
Considere, abaixo, as espécies iônicas e as metodologias utilizadas para remoção dessas espécies no tratamento de efluentes industriais.
|
Espécie Iônica |
Metodologia |
|
| I | \( CrO_4^{-2} \) |
Redução com FeSO4 em meio ácido, seguida |
| II | \( CN^- \) |
Reação com NaClO em meio alcalino, com |
| III | \( PO_4^{-3} \) |
Adição de FeCl3 ou Al2(SO4)3, com formação |
A relação entre a espécie iônica e a metodologia utilizada está correta em:
Provas
A figura abaixo corresponde a uma curva titrimétrica onde se relaciona a variação do pH em função do volume do titulante.
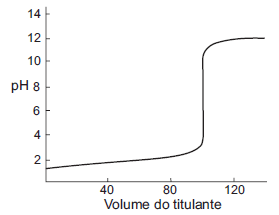
Considerando-se que titulante e titulado possuem concentração 0,1 mol/L e que o volume do titulado é de 100 mL, o sistema que é compatível com esta curva é o:
| Titulado |
Titulante |
Provas
Considere as seguintes afirmações relacionadas à técnica analítica de espectroscopia de absorção atômica:
I - sais de potássio são freqüentemente utilizados como supressores de ionização na amostra problema, devido à baixa energia de ionização deste elemento;
II - nas determinações de cálcio, a presença dos íons sulfato e fosfato na amostra diminuem a extensão da atomização do analito, devido à formação de sais não voláteis;
III - supressores de ionização são espécies facilmente ionizáveis que reprimem a ionização do analito através do fornecimento de uma grande concentração de elétrons na chama;
IV - tampões de radiação consistem de reagentes que formam complexos voláteis estáveis com o analito, evitando, deste modo, interferências por ânions que possam formar compostos não voláteis com o elemento de interesse.
Estão corretas as afirmações:
Provas
Três laboratoristas efetuaram análises titrimétricas em replicata para padronizar uma solução 0,1 mol/L de NaOH. Para tal, retiraram uma alíquota de exatamente 10,00 mL da solução de NaOH e titularam contra uma solução 0,10 mol/L de HCl previamente padronizada. Os resultados das análises estão listados na tabela abaixo.
|
Laboratorista |
Volume de HCl (mL) |
Média |
Coeficiente de |
| I |
10,08 10,11 10,09 10,11 |
10,10 |
0,15 |
| II |
9,88 10,14 10,02 9,80 |
9,96 |
1,51 |
| III |
10,19 9,79 9,69 9,78 |
9,86 |
2,26 |
O resultado mais preciso e o resultado mais exato foram obtidos, respectivamente, pelos laboratoristas:
Provas
O fósforo pode ser obtido a partir da reação do fosfato de cálcio com areia e coque, conforme a reação abaixo. Fosfato de cálcio + Areia + C ![]() CaSiO3 + Monóxido de carbono + P4
CaSiO3 + Monóxido de carbono + P4
A reação completa de 124 g de fosfato de cálcio produz uma quantidade de monóxido de carbono que, nas condições normais de temperatura e pressão, corresponde a um volume, em litros, de: (Dados: Volume molar dos gases = 22,4 L, a 1atm e 0 ºC)
Provas
A aparelhagem abaixo foi utilizada com sucesso na separação dos compostos A e B.
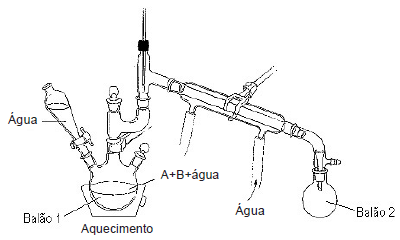
A respeito dessa operação básica de laboratório, é correto afirmar que:
Provas
Uma barra metálica de zinco foi ligada a uma tubulação subterrânea para protegê-la contra a corrosão. A respeito dessa proteção, é correto afirmar que:
Provas
Cem mililitros de solução aquosa 0,1 mol/L de HCl foram acrescentados a três frascos que continham, respectivamente:
I - 400 mL de H2O;
II - 200 mL de solução 0,4 mol/L de HCl;
III - 100 mL de solução aquosa 0,1 mol/L de NaOH.
Em seguida, as três soluções foram misturadas. O pH da solução resultante será:
Provas
O número total de elétrons desemparelhados existentes nas espécies 8O, O2 e 8O-2 é:
[Dados: ordem crescente de energia dos orbitais moleculares de moléculas diatômicas ( \( \sigma \)1s < \( \sigma \)*1s < \( \sigma \)2s < \( \sigma \)*2s < \( \sigma \)2pZ < \( \pi \)2pX = \( \pi \)2pY < \( \pi \)*2pX = \( \pi \)*2pY < \( \sigma \)*2pZ ...)]
Provas
Caderno Container