Foram encontradas 80 questões.
Considere as substâncias a seguir.
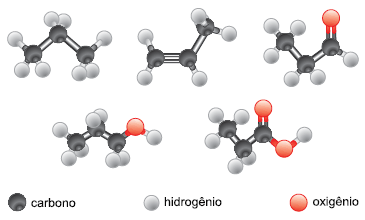
A substância que consome a menor quantidade de oxigênio em sua combustão completa é
Provas
O iodo é um elemento relativamente raro, cuja forma elementar (I2) é produzida a partir de suas espécies iônicas encontradas na natureza. As algas marinhas e as águas-mães do processamento do salitre do Chile são fontes naturais de íons iodeto (I–) e iodato (IO3–), respectivamente. A conversão desses íons em iodo molecular ocorre de acordo com as equações 1 e 2.
Equação 1:
MnO2 + 2KI + 2H2SO4 → Mn2+ + I2 + 2K+ + 2H2O + 2SO4 2–
Equação 2:
2IO3 – + 5NaHSO3 → I2 + 5Na+ + 3H+ + 5SO4 2– + H2O
De acordo com os processos descritos, o elemento iodo sofre
Provas
Considere as equações químicas:
I. N2O4 (g) \( \rightleftharpoons \) 2NO2 (g)
II. CaO (s) + CO2 (g) \( \rightleftharpoons \) CaCO3 (s)
III. NH4Cℓ (s)\( \rightleftharpoons \) NH3 (g) + HCℓ (g)
IV. Sn (s) + H2 (g) \( \rightleftharpoons \) Sn (s) + H2O (g)
V. 4Aℓ (s) + 3O2 (g) \( \rightleftharpoons \) 2Aℓ2O3 (s)
Considerando x um dos compostos químicos presentes nas equações citadas, a expressão da constante de equilíbrio representada por \( K_p={\large{1 \over p(x)}} \) descreve corretamente o equilíbrio representado na equação
Provas
O fenol é uma substância de caráter ácido, que sofre ionização de acordo com a equação a seguir.
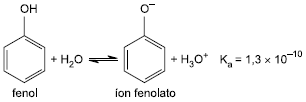
Com base nessas informações, pode-se afirmar que:
Provas
O etanol (C2H6O) pode ser produzido em laboratório por meio da hidratação do etileno (C2H4), conforme a equação:
C2H4 + H2O → C2H6O
A entalpia dessa reação pode ser calculada por meio da Lei de Hess, utilizando-se as equações:
C2H4 + 3O2 → 2CO2 + 2H2O ΔH = – 1 322 kJ/mol de C2H4
C2H6O + 3O2 → 2CO2 + 3H2O ΔH = – 1 367 kJ/mol de C2H6O
Com base nas informações fornecidas, a produção de 10 mol de etanol
Provas
A mistura de 100 mL de uma solução de HCℓ, de concentração 2 x 10 –2 mol/L, com 400 mL de uma solução de NaOH, de concentração 6,25 x 10 –3 mol/L, gera uma solução de caráter
Provas
Amostras das substâncias cloreto de potássio (KCℓ), cloreto de amônio (NH4Cℓ), clorofórmio (CHCℓ3) e sacarose (C12H22O11) foram colocadas, separadamente e não necessariamente nessa ordem, em quatro tubos de ensaio contendo água, identificados de 1 a 4. Cada sistema formado foi submetido a testes de condutividade elétrica e pH. Os resultados foram reunidos na tabela a seguir.
|
Tubo |
Classificação do sistema | O sistema é condutor de corrente elétrica? |
pH |
| 1 | homogêneo | sim |
4,5 |
| 2 | heterogêneo |
não |
--- |
| 3 | homogêneo | sim |
7,0 |
| 4 | homogêneo | não |
7,0 |
As substâncias adicionadas aos tubos 1, 2, 3 e 4 foram, respectivamente,
Provas
O oxigênio é o produto gasoso da reação de decomposição do clorato de potássio (KCℓO3), de acordo com a equação:
2KCℓO3 → 2KCℓ + 3O2
Considerando a constante universal dos gases igual a 0,082 atm · L · mol –1 · K –1, o volume de gás oxigênio produzido na decomposição de 0,5 mol de clorato de potássio a 1 atm e 400 K é igual a
Provas
A natureza das ligações intermoleculares define as propriedades das substâncias. Ocorre quebra de ligações intermoleculares em uma substância simples no processo representado pela equação:
Provas
Lâmpadas de neon são tubos contendo gases rarefeitos submetidos a uma diferença de potencial. Quando elétrons percorrem o tubo, colidem com as moléculas do gás e emitem luz com cor característica do elemento químico, conforme ilustra a figura.

(www.fart-neon.com)
A natureza da luz emitida pelas lâmpadas de neon pode ser explicada pelos modelos atômicos de
Provas
Caderno Container