Foram encontradas 90 questões.
A adição de um soluto não volátil em um solvente puro provoca o abaixamento de sua pressão de vapor e, em consequência, sua temperatura de ebulição é alterada.
Um estudante resolveu medir, no laboratório, as temperaturas de ebulição de quatro soluções aquosas, todas de concentração 0,5 mol.L–1, e compará-las com a da água pura, como mostrado a seguir.
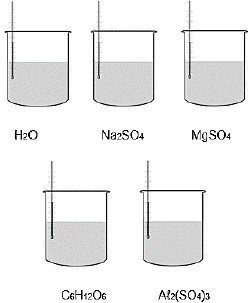
Com relação aos resultados obtidos pelo estudante, assinale a afirmativa correta.
Provas
Um grupo de cisnes ficou viciado em ópio depois de terem entrado em um campo de papoulas na Eslováquia. É possível que os cisnes tenham chegado ao campo quando um lago temporário se formou lá após fortes chuvas. Outra possibilidade é a de que eles tenham confundido os pés de papoula, que tem um látex usado para produzir anestésicos viciantes, com colza, uma das plantas favoritas das aves.
Adaptado de: https://oglobo.globo.com/mundo/epoca/noticia/2023/06/cisnesinvadem- campo-de-papoulas-e-ficam-viciados-em-opio-na-eslovaquiaentenda. ghtml?utm_source=aplicativoOGlobo&utm_medium=aplicativo&utm_cam paign=compartilhar. Acesso em 22/07/2023.
Analise a seguir as estruturas de três compostos presentes no látex das papoulas.
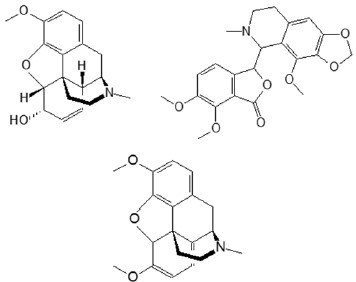
As funções orgânicas comuns aos três compostos são
Provas
Uma mineradora da Noruega anunciou a descoberta de uma reserva gigante de rocha fosfática, capaz de suprir a demanda global de fertilizantes e carros elétricos pelos próximos 50 anos.
A rocha fosfática é usada para produzir fósforo, ingrediente crucial para a produção de fertilizantes. Ela também pode ser processada para se transformar em ácido fosfórico, que pode ser utilizado nas baterias de lítio-ferro-fosfato que alimentam sistemas de energia solar e carros elétricos.
Disponível em: https://oglobo.globo.com/economia/noticia/2023/07/10/ mineradora-da-noruega-descobre-deposito-de-minerais-que-pode-abastecercarros- eletricos-por-50-anos.ghtml. Acesso em 24/07/2023.
Na produção de ácido fosfórico, uma rocha fosfática constituída exclusivamente por Ca10(PO4)6F2 foi tratada com ácido sulfúrico, produzindo sulfato de cálcio hidratado, ácido fluorídrico e ácido fosfórico de acordo com a reação química:
Ca10(PO4)6F2 (s) + 10 H2SO4 (aq) + 20 H2O (\( l \)) → 10 CaSO4 . 2H2O (s) + 2 HF (aq) + 6 H3PO4 (aq)
Em condições adequadas foram obtidos 588kg de ácido fosfórico a partir de 2,016 toneladas de rocha fosfática. Considerando a equação química balanceada apresentada, o rendimento do processo foi de, aproximadamente,
Dados: massas molares (g.mol–1): Ca10(PO4)6F2 = 1008; H3PO4 = 98
Provas
Considere que um metal pesado é o nome genérico utilizado para indicar todo metal com densidade acima de 6,0g/cm3.
Na forma metálica, esses metais não são solúveis em água. No entanto a chuva ácida reage com esses metais tornando-os substâncias solúveis e liberando cátions que podem atingir águas subterrâneas, gerando problemas de poluição ambiental.
Observe a tabela com as massas e os volumes ocupados por 5 (cinco) metais.
|
Metal |
Massa (g) |
Volume (cm3) |
|
Alumínio |
81,00 | 30 |
|
Bário |
144,00 | 40 |
|
Cádmio |
435,00 | 50 |
|
Lítio |
10,60 | 20 |
|
Magnésio |
17,40 | 10 |
De acordo com o texto, assinale a opção que indica o cátion do metal que, ao reagir com a chuva ácida, pode provocar poluição ambiental nas águas subterrâneas.
Provas
Veículos totalmente elétricos e híbridos utilizam baterias que contém lítio, semelhantes às utilizadas em notebooks e smartphone, nas quais a grande vantagem é o fato de não terem efeito de memória e serem livres de manutenção. Existem diferentes métodos para obtenção e purificação do lítio, como por exemplo, o processo eletrolítico.
Nesse processo, para se obter 700mg de lítio metálico, utilizando uma corrente de 5 Ampères, o tempo necessário, em minutos, é de, aproximadamente,
Dado: massa molar do lítio = 7 g.mol–1; 1F = 96500 Coulomb.
Provas
Ácidos orgânicos têm sido utilizados como esfoliantes químicos para promover a renovação celular e colaborar com a administração de substâncias que atuam estimulando a produção de colágeno e elastina, permitindo a renovação da pele. O pH da solução ácida influencia diretamente no efeito esperado.
Uma solução diluída de concentração 0,01 mol.L–1 de um monoácido orgânico fraco com pKa = 4, utilizado em um processo de esfoliação, apresenta pH aproximadamente igual a
Provas
A Agência Internacional de Pesquisa sobre o Câncer (IARC, da sigla em inglês), braço da Organização Mundial da Saúde (OMS), resolveu incluir o aspartame como substância ‘possivelmente cancerígena’ embora os estudos sejam limitados.
https://oglobo.globo.com/saude/medicina/noticia/2023/07/14/aspartame
A OMS, no entanto, manteve o limite de ingestão diário (IDA) de 40 mg de aspartame por quilo de peso corporal como índice seguro, com base nas evidências atuais.
Uma lata de refrigerante zero, de 350mL contém, em média, 42mg de aspartame. Se um indivíduo, pesando 75kg, ingerir 4 latas desse refrigerante em um único dia, sendo essa a sua única fonte de aspartame, é correto afirmar que ele estará, aproximadamente,
Provas
A configuração eletrônica de um átomo é importante pois determina suas propriedades químicas. Observe as distribuições eletrônicas compactas de dois átomos, X e Y:
X: [Ne] 3s2 3p5
Y: [He] 2s2 2p4
Suponha que X e Y se ligam formando um composto, em que X apresenta seu maior número de oxidação. Este composto, por sua vez, sofre uma reação de hidratação.
Assinale a opção que indica a fórmula química e o nome do composto formado na reação química de hidratação, respectivamente.
Provas
O carbono-14 é um isótopo muito usado para datar materiais orgânicos. Porém, os geólogos precisam de outros materiais para determinar a idade de rochas mais antigas. Um dos radioisótopos utilizados é o potássio-40, cuja meia-vida é de 1,26Ga (1 Ga= 109 anos).
Sabendo que o potássio-40 se desintegra por captura de um elétron, o tempo necessário para que 75% de uma amostra se desintegre e o número de nêutrons do elemento químico formado nesse processo, são, respectivamente,
Dado: Número atômico do potássio= 19.
Provas
Em 1815, as tropas napoleônicas foram definitivamente derrotadas na Europa. Esse fato criou condições políticas para o retorno da família real à metrópole. No entanto, D. João não tomou qualquer iniciativa nesse sentido. Ao contrário, tratou de reforçar a presença da Corte na América, elevando a colônia a Reino Unido a Portugal e Algarves. Tal medida não somente colocou a até então colônia em um outro patamar de importância político-administrativa, como reforçou a posição dos grupos que defendiam junto ao príncipe a transferência definitiva da sede do Império para o Rio de Janeiro.
História em curso: o Brasil e suas relações com o mundo ocidental. São Paulo: Editora do Brasil; Rio de Janeiro: FGV, 2004
A respeito do governo joanino e da independência brasileira, analise as afirmativas a seguir.
I. O maior desafio enfrentado por D. João em sua estada na América foi a rebelião de Pernambuco (1817), um movimento de reação à política joanina que se espalhou pelas capitanias vizinhas, reativas ao aumento de impostos para a manutenção da Corte no Rio de Janeiro.
II. Em 1820, uma série de revoltas contra o absolutismo monárquico eclodiram em Portugal, sendo vitoriosas na cidade do Porto, onde exigiu-se a extinção da monarquia dos Bragança e a elaboração de uma Constituição republicana.
III. A reação de D. João à revolução do Porto foi permanecer em terras americanas e assegurar a continuação de sua dinastia e de seu governo para o herdeiro, o príncipe D. Pedro, que assumiria o processo formal de independência a partir do Rio de Janeiro.
Está correto o que se afirma em
Provas
Caderno Container