Foram encontradas 40 questões.
Observe as afirmativas abaixo sobre a caracterização de metabólitos formados a partir de substâncias inovadoras.
I. A precisão nas medidas de massa e informações valiosas sobre fragmentação fornecidas pela espectrometria de massa de alta resolução (HR-MS) contribuem significativamente para a caracterização do metabólito.
II. A identificação de metabólitos em humanos e ratos deve ser investigada na fase inicial do desenvolvimento do medicamento para avaliação da biodisponibilidade.
III. A cromatografia líquida de ultra eficiência/espectrometria de massa de tempo de voo quadrupolo (UHPLC/Q-TOF MS) pode ser utilizada para rastrear e caracterizar os metabólitos em plasma, urina e fezes de humanos e de ratos.
Das afirmativas acima:
I. A precisão nas medidas de massa e informações valiosas sobre fragmentação fornecidas pela espectrometria de massa de alta resolução (HR-MS) contribuem significativamente para a caracterização do metabólito.
II. A identificação de metabólitos em humanos e ratos deve ser investigada na fase inicial do desenvolvimento do medicamento para avaliação da biodisponibilidade.
III. A cromatografia líquida de ultra eficiência/espectrometria de massa de tempo de voo quadrupolo (UHPLC/Q-TOF MS) pode ser utilizada para rastrear e caracterizar os metabólitos em plasma, urina e fezes de humanos e de ratos.
Das afirmativas acima:
Provas
Questão presente nas seguintes provas
É crucial para o desenvolvimento inicial de medicamentos realizar perfis metabólicos em uma nova entidade química.
A figura abaixo apresenta os espectros de massa MS/MS da BH, um inibidor do transportador Na+/Ca2+ da superfície da
membrana.
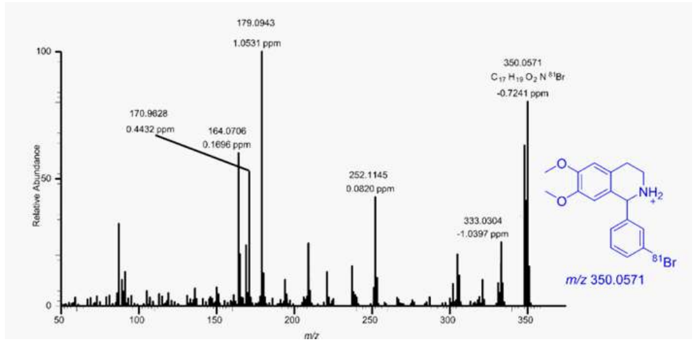
Observe as afirmativas a seguir sobre o metabolismo de fármacos.
I. BH é o composto original de todos os seus metabólitos, e, como os metabólitos derivam do BH, as características espectrais de massa dos metabólitos apresentam altas correlações com as do BH.
II. O fragmento mais abundante, o íon em m/z 179,0943, foi produzido pela perda de um radical metila e da 3’-bromo benzeno.
III. O pico do íon molecular protonado de BH no modo positivo ESI foi m/z 350,0571 (C17H19O2N 81Br).
Das afirmativas acima:

Observe as afirmativas a seguir sobre o metabolismo de fármacos.
I. BH é o composto original de todos os seus metabólitos, e, como os metabólitos derivam do BH, as características espectrais de massa dos metabólitos apresentam altas correlações com as do BH.
II. O fragmento mais abundante, o íon em m/z 179,0943, foi produzido pela perda de um radical metila e da 3’-bromo benzeno.
III. O pico do íon molecular protonado de BH no modo positivo ESI foi m/z 350,0571 (C17H19O2N 81Br).
Das afirmativas acima:
Provas
Questão presente nas seguintes provas
Um medicamento fitoterápico com ação antioxidativa, anti-inflamatória, antiproliferativa, antitumoral, antimicrobiana
e anti-Alzheimer, tem sido amplamente utilizado para o tratamento de reumatismo e alívio da dor na China. No entanto,
as características farmacocinéticas incluindo a biodisponibilidade deste composto permanecem indefinidas. Os gráficos
abaixo apresentam as curvas da média da concentração plasmática desse fitoterápico em escala logarítmica ordenada
(n = 8): (A) administração intravenosa do fitoterápico 2,5, 5, 10 mg/Kg; (B) administração oral do fitoterápico 20 mg/Kg. A
tabela abaixo mostra a média dos parâmetros farmacocinéticos estimados do fitoterápico após administração intravenosa
(i.v.) e oral (i.g.) (n = 8).
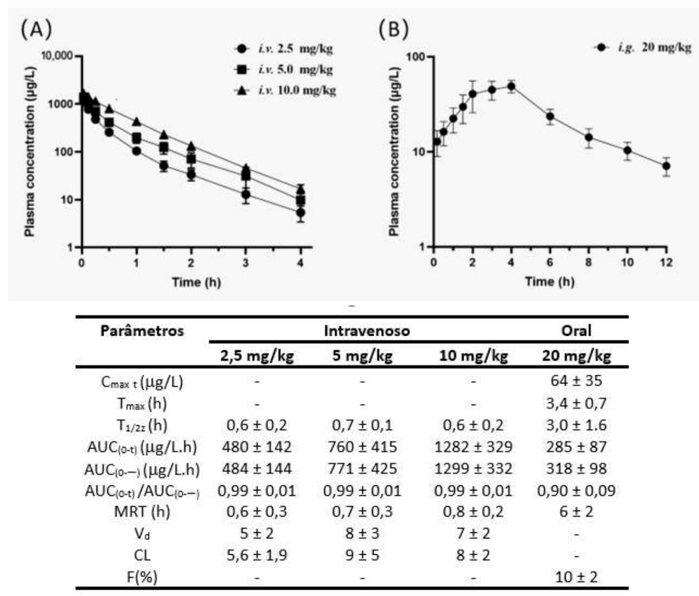
Cmax (pico da concentração plasmática máxima), Tmáx (o tempo para atingir o pico de concentração); AUC(0–t) (área sob a curva desde o tempo zero até o último ponto de amostragem); AUC(0–∞) (área sob a curva do tempo zero ao infinito); MRT (tempo médio de residência); T1/2Z (tempo de meia vida de eliminação); VZ (volume de distribuição aparente); F (biodisponibilidade).
Observe as afirmativas abaixo sobre os gráficos e tabela:
I. Para todos os perfis concentração-tempo no estudo, a proporção de AUC(0–t) para AUC(0–∞) foi superior a 90%.
II. Os perfis farmacocinéticos após a administração intravenosa na dose de 2,5, 5 e 10 mg/kg mostrou meia-vida de eliminação média semelhante (T1/2 de 0,6~0,7 h), tempo médio de residência (MRT de 0,6~0,80 h), volume de distribuição (Vd de 5~7 L/kg) e depuração sistêmica (CL de 5,6~9 L/kg/h), que não apresentaram diferenças entre os diferentes níveis de dose (p > 0,05).
III. A biodisponibilidade absoluta do fitoterápico após dose única (20 mg/kg) foi de cerca de 10± 2%, indicando boa absorção do fitoterápico em ratos.
Das afirmativas acima:

Cmax (pico da concentração plasmática máxima), Tmáx (o tempo para atingir o pico de concentração); AUC(0–t) (área sob a curva desde o tempo zero até o último ponto de amostragem); AUC(0–∞) (área sob a curva do tempo zero ao infinito); MRT (tempo médio de residência); T1/2Z (tempo de meia vida de eliminação); VZ (volume de distribuição aparente); F (biodisponibilidade).
Observe as afirmativas abaixo sobre os gráficos e tabela:
I. Para todos os perfis concentração-tempo no estudo, a proporção de AUC(0–t) para AUC(0–∞) foi superior a 90%.
II. Os perfis farmacocinéticos após a administração intravenosa na dose de 2,5, 5 e 10 mg/kg mostrou meia-vida de eliminação média semelhante (T1/2 de 0,6~0,7 h), tempo médio de residência (MRT de 0,6~0,80 h), volume de distribuição (Vd de 5~7 L/kg) e depuração sistêmica (CL de 5,6~9 L/kg/h), que não apresentaram diferenças entre os diferentes níveis de dose (p > 0,05).
III. A biodisponibilidade absoluta do fitoterápico após dose única (20 mg/kg) foi de cerca de 10± 2%, indicando boa absorção do fitoterápico em ratos.
Das afirmativas acima:
Provas
Questão presente nas seguintes provas
Um inibidor altamente específico de CDK4 e CDK6, biodisponível por via oral, demonstrou uma tolerabilidade controlável e potencial terapêutico para uma variedade de tipos de câncer. Dados pré-clínicos sugerem que esse inibidor
pode atravessar a barreira hematoencefálica, apoiando o desenvolvimento clínico adicional do tratamento de tumores
do sistema nervoso central. A análise de amostras de plasma, tumor e líquido cefalorraquidiano (LCR) foi realizada para
avaliar a farmacocinética e a penetração do composto no sistema nervoso central e no tumor.
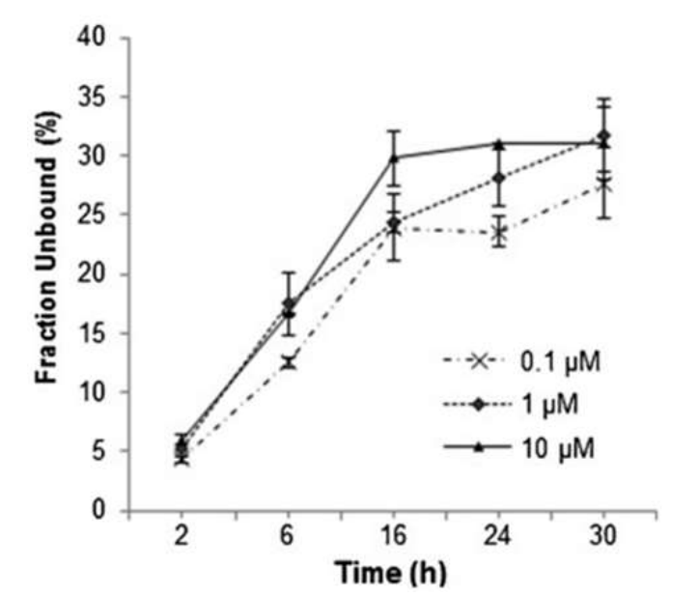
Observe as afirmativas abaixo sobre o gráfico acima: fração não ligada do inibidor (0,1, 1 e 10 μM) no plasma no tempo de equilíbrio de 2, 4, 6, 16 e 24 h.
I. A fração não ligada do inibidor no plasma pode ser determinada por diálise de equilíbrio.
II. O tempo de equilíbrio otimizado da fração não ligada do inibidor no plasma é de 6 h.
III. O inibidor ligou pouco às proteínas plasmáticas.
Das afirmativas acima:

Observe as afirmativas abaixo sobre o gráfico acima: fração não ligada do inibidor (0,1, 1 e 10 μM) no plasma no tempo de equilíbrio de 2, 4, 6, 16 e 24 h.
I. A fração não ligada do inibidor no plasma pode ser determinada por diálise de equilíbrio.
II. O tempo de equilíbrio otimizado da fração não ligada do inibidor no plasma é de 6 h.
III. O inibidor ligou pouco às proteínas plasmáticas.
Das afirmativas acima:
Provas
Questão presente nas seguintes provas
Sobre os estudos de farmacocinética para otimizar a dose e o regime de dosagem de um composto, é INCORRETO
afirmar que:
Provas
Questão presente nas seguintes provas
C118P, um pró-fármaco com o grupo éster fosfato de C118, que é um novo inibidor de proteína de microtúbulos, está
atualmente em desenvolvimento clínico de Fase I na China para o tratamento de câncer de ovário e câncer de pulmão.
Os gráficos mostram os perfis de concentração plasmática versus tempo de C118P em ratos (A), C118 em ratos (B),
após a administração intravenosa de doses 5, 10, 20 e 50 mg/kg de C118P.
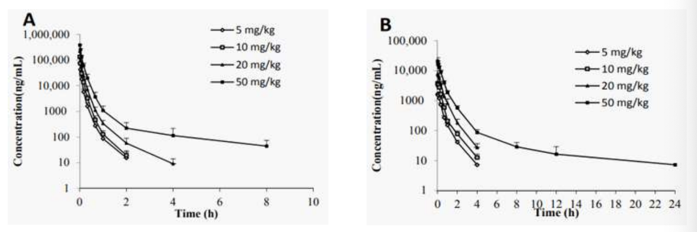
Observe as afirmativas a seguir:
I. Tanto C118P quanto C118 foram detectáveis no plasma de ratos após administração por via intravenosa de C118P.
II. Após a administração intravenosa, C118P pode ser hidrolisado em C118 rapidamente, com C118P e C118 detectáveis no sangue simultaneamente.
III. A área sob a curva de C118 reduziu proporcionalmente a dose no intervalo de 5–50 mg/kg.
Das afirmativas acima:

Observe as afirmativas a seguir:
I. Tanto C118P quanto C118 foram detectáveis no plasma de ratos após administração por via intravenosa de C118P.
II. Após a administração intravenosa, C118P pode ser hidrolisado em C118 rapidamente, com C118P e C118 detectáveis no sangue simultaneamente.
III. A área sob a curva de C118 reduziu proporcionalmente a dose no intervalo de 5–50 mg/kg.
Das afirmativas acima:
Provas
Questão presente nas seguintes provas
Um novo protótipo antineoplásico foi desenvolvido com mecanismo de morte de células leucêmicas K562, através
de sinalização necroptótica. Devido ao seu efeito promissor, estudos sobre a sua farmacocinética foram realizados utilizando um novo método bioanalítico validado, baseado em cromatografia líquida acoplada à espectrometria de massas
sequencial. A tabela abaixo apresenta a média dos parâmetros farmacocinéticos desse novo protótipo em ratos (n = 3)
após administração intraperitoneal na dose de 100 mg/kg.
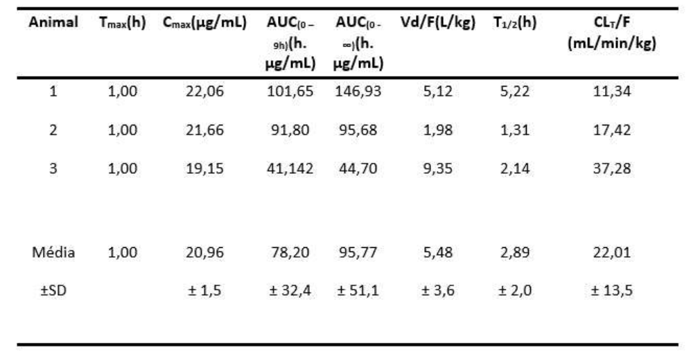
Tmáx (o tempo para atingir o pico de concentração); Cmax (pico da concentração plasmática máxima), AUC(0–9) (área sob a curva desde o tempo zero até 9h); AUC(0 - ∞) (área sob a curva do tempo zero ao infinito); MRT (tempo médio de residência); Vd/F (volume de distribuição aparente); T1/2 (tempo de meia vida de eliminação); F (biodisponibilidade); CL (Clearence).
Sobre os estudos do novo protótipo, é INCORRETO afirmar que:

Tmáx (o tempo para atingir o pico de concentração); Cmax (pico da concentração plasmática máxima), AUC(0–9) (área sob a curva desde o tempo zero até 9h); AUC(0 - ∞) (área sob a curva do tempo zero ao infinito); MRT (tempo médio de residência); Vd/F (volume de distribuição aparente); T1/2 (tempo de meia vida de eliminação); F (biodisponibilidade); CL (Clearence).
Sobre os estudos do novo protótipo, é INCORRETO afirmar que:
Provas
Questão presente nas seguintes provas
Observe as afirmativas a seguir sobre os estudos de metabolismo de medicamentos:
I. Durante o processo de desenvolvimento de medicamentos para avaliar o risco da interação de fármaco - fármaco baseados em citocromo CYP450 -, o primeiro tipo de estudo consiste em identificar a via metabólica do novo medicamento e a capacidade de outras moléculas terapêuticas pretendidas modificarem o metabolismo do novo medicamento.
II. Estudos mais complexos avaliam a possibilidade de o novo medicamento alterar o metabolismo de outros medicamentos.
III. As enzimas citocromo (CYP) do fígado metabolizam uma ampla gama de medicamentos, e mais de 90% das interações de fármaco - fármaco acontecem na etapa catalisada pela enzima CYP.
Das afirmativas acima:
I. Durante o processo de desenvolvimento de medicamentos para avaliar o risco da interação de fármaco - fármaco baseados em citocromo CYP450 -, o primeiro tipo de estudo consiste em identificar a via metabólica do novo medicamento e a capacidade de outras moléculas terapêuticas pretendidas modificarem o metabolismo do novo medicamento.
II. Estudos mais complexos avaliam a possibilidade de o novo medicamento alterar o metabolismo de outros medicamentos.
III. As enzimas citocromo (CYP) do fígado metabolizam uma ampla gama de medicamentos, e mais de 90% das interações de fármaco - fármaco acontecem na etapa catalisada pela enzima CYP.
Das afirmativas acima:
Provas
Questão presente nas seguintes provas
O composto CA apresentou atividade terapêutica promissora contra doenças metabólicas, incluindo demência e
osteoporose, e apresentou também efeito antibacteriano, antioxidante, anti-hipertensivo e antidiabético. A tabela abaixo
apresenta os parâmetros farmacocinéticos de CA no plasma de ratos Sprague Dawley (SD) machos após administração
oral (100 mg/kg, n=5, média ± DP) e intravenosa (10 mg/kg, n=5, média ± DP). Observe os parâmetros farmacocinéticos
do CA:
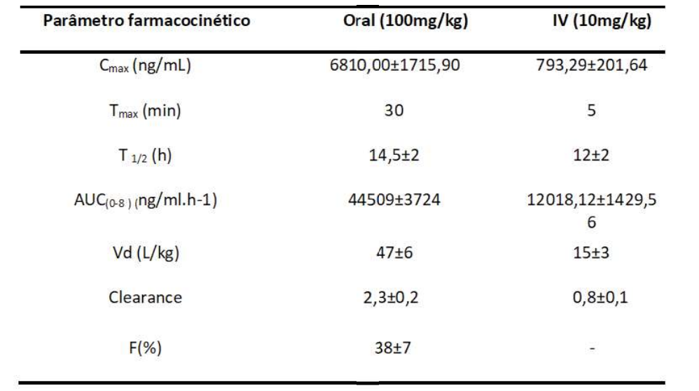
Cmax (pico da concentração plasmática máxima), Tmáx (o tempo para atingir o pico de concentração); T1/2 (tempo de meia vida de eliminação); AUC(0–∞) (área sob a curva do tempo zero ao infinito); Vd (volume de distribuição aparente); CL (Clearance); F (biodisponibilidade).
Sobre o assunto é possível afirmar que:
I. Uma taxa mais lenta de eliminação e depuração significa uma presença prolongada de CA na circulação sistêmica, conduzindo potencialmente a efeitos farmacológicos sustentados e desejáveis.
II. Um maior volume de distribuição e uma menor depuração conduzem a uma redução da meia-vida, o que também terá impacto na eficácia terapêutica da CA.
III. A biodisponibilidade absoluta do CA foi 38%, o que desempenha um papel crítico na determinação do regime de dosagem do CA e está intimamente relacionado com outros parâmetros farmacocinéticos primários, incluindo meia-vida e depuração.
Das afirmativas acima:

Cmax (pico da concentração plasmática máxima), Tmáx (o tempo para atingir o pico de concentração); T1/2 (tempo de meia vida de eliminação); AUC(0–∞) (área sob a curva do tempo zero ao infinito); Vd (volume de distribuição aparente); CL (Clearance); F (biodisponibilidade).
Sobre o assunto é possível afirmar que:
I. Uma taxa mais lenta de eliminação e depuração significa uma presença prolongada de CA na circulação sistêmica, conduzindo potencialmente a efeitos farmacológicos sustentados e desejáveis.
II. Um maior volume de distribuição e uma menor depuração conduzem a uma redução da meia-vida, o que também terá impacto na eficácia terapêutica da CA.
III. A biodisponibilidade absoluta do CA foi 38%, o que desempenha um papel crítico na determinação do regime de dosagem do CA e está intimamente relacionado com outros parâmetros farmacocinéticos primários, incluindo meia-vida e depuração.
Das afirmativas acima:
Provas
Questão presente nas seguintes provas
“Para obter resultados quantitativamente significativos
sem as substâncias padrão dos analitos identificados, uma
série de estratégias diferentes vem sendo desenvolvidas
em análises não-direcionadas por cromatografia líquida
acoplada à espectrometria de massas de alta resolução
(LC-HRMS).” (KRUVE, A. Anal. Chem. 2020;92:4691-4699)
Segundo Kruve (2020), algumas das abordagens mais empregadas são as abaixo relacionadas, EXCETO:
Segundo Kruve (2020), algumas das abordagens mais empregadas são as abaixo relacionadas, EXCETO:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container