Foram encontradas 65 questões.
Em água, comporta-se como uma base de Brönsted-Lowry:
Provas
Um elemento X apresenta como subnível mais energético o subnível “p” onde dois orbitais atômicos deste encontram-se totalmente preenchidos e sendo localizado no terceiro período da tabela. Sobre este elemento, é correto afirmar que:
Provas
Um acadêmico de química foi incumbido de realisar experiências e anotar dados em uma tabela relacionando concentração dos reagentes(A e B) e a velocidade de reação. Obteve os seguintes resultados
| Concentração/(mol . L-1) | Velocidade (mol . L-1 . min -1) | |
| [A] | [B] | |
| 1,0 |
1,0 |
0,15 |
| 2,0 |
1,0 |
0,30 |
| 3,0 |
1,0 |
0,45 |
|
1,0 |
2,0 |
0,15 |
|
1,0 |
3,0 |
0,15 |
Analisando os resultados das reações, conclui-se que a equação da velocidade de reação é dada por:
Provas
Uma solução de carbonato de sódio foi preparada dissolvendo 2,65g deste sal em água suficiente para prepara 250 ml de solução. Sabendo que o íon carbonato se hidrolisa segundo a equação:
CO3 -2 (aq)+ H2O ( l ) \( → \) HCO3 – ( aq ) + OH – ( aq )
Se formos medir o pH dessa solução, iríamos encontrar o valor de :
Dados: M. molar em g/mol Na=23, C=12 e O=16 ; Kh = 2,5 x 10 -4 mol/L ; log 5 = 0,69; Kw=1x10 -14.
Provas
Sobre a estrutura dos átomos e suas partículas, são feitas as afirmações:
I – O átomo é formado por três pequenas partículas indivisíveis e indestrutíveis denominadas elétrons, prótons e nêutrons.
II – Os átomos, apesar de serem indivisíveis, são constituídos por elétrons, prótons e nêutrons.
III – Quando um elétron passa de um estado estacionário de baixa energia para um de alta energia, há a emissão de radiação (energia).
IV – O átomo é constituído por um núcleo contendo prótons e nêutrons, rodeado por elétrons que circundam em órbitas estacionárias.
Estão corretas:
Provas
Com um conta-gotas determinou-se que são necessários 20 gotas para completar 1 ml. Em 1 gota de ácido clorídrico 0,0001mol/L encontramos:
Provas
Dados os números atômicos dos átomos de lítio (Li = 3), flúor (F = 9), enxofre (S = 16) e cloro (Cl = 17), assinale os tipos de Iigação química que estão presentes nos compostos LiF, SCI2 e Cl2, respectivamente.
Provas
Na bula de um frasco de dipirona sódica encontra-se:
Composição da Dipirona Sódica:
gotas com 0,5 g/ml de dipirona sódica e soluçãoinjetável com 0,5 g/ml de dipirona sódica.
Posologia e Administração da Dipirona Sódica:
gotas: adultos: 20 a 40 gotas, até 3 vezes por dia. Lactentes e crianças menores de 5 anos: 4 a 8 gotas, até 4 vezes por dia. Crianças maiores de 5 anos: 10 a 20 gotas, até 4 vezes ao dia. Solução injetável: adulto: a critério médico. Em média 1 a 4 ampolas por dia.
Indicações da Dipirona Sódica:
Analgésico e antipirético. www.bulas.med.br
O valor aproximado da concentração em mol/L para a dipirona sódica (C13H16N3O4SNa) é: ( M. atômica em g/mol: C=12, H=1, N=14, O=16, S=32 e Na=23)
Provas
Um estudante do ensino médio ao ler num pote de requeijão cremoso, verificou que era composto por: “Leite padronizado reconstituído, creme de leite, soro de leite, caseinato de cálcio, água, sal, cloreto de cálcio, fermentos lácteos, enzima protease, estabilizantes polifosfato de sódio e difosfato de sódio, conservante sorbato de potássio. Não Contém Glúten.” Curioso em saber o que era sorbato de potássio, pesquisou e encontrou a fórmula:
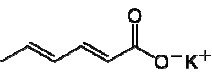
E afirmou que:
I – É um produto do reação do ácido sórbico com hidróxido de potássio.
II – Todos seus carbono são insaturados.
III – Sua fórmula molecular é C6 H7 K O2 .
Das afirmações do estudante:
Provas
Sobre radioatividade são feitas as seguintes afirmações:
I – A perda de uma partícula beta pelo átomo de 53 135 Iobtemos um isótopo do iodo.
II – Quando um núcleo emite uma partícula alfa seu número atômico diminui em duas unidades.
III – Na transformação do átomo 89 228Ac em 84 212 Po são emitidas 4 partículas alfa e 3 partículas beta.
Das afirmações:
Provas
Caderno Container