Foram encontradas 50 questões.
Um técnico de laboratório de química utilizou a mesma quantidade de matéria de solutos não voláteis no preparo de três soluções (de volumes idênticos), denominadas A, B e C, cujos solutos são, respectivamente, hidróxido de sódio, propan-1,2,3-triol e fosfato de sódio. Essas soluções foram submetidas ao aquecimento, separadamente, até que atingissem a temperatura de ebulição (T). Considere que essas soluções possuem comportamento ideal e que a mesma massa de solvente foi usada no preparo de cada solução.
A relação entre a temperatura de ebulição das soluções A, B e C é
Provas
Para que uma análise química volumétrica seja validada devemos conhecer exatamente a quantidade de um dos reagentes usados. Dessa forma, determinamos a concentração de uma solução-problema a partir de sua reação quantitativa com uma quantidade conhecida de uma substância que é pura, chamada de padrão primário.
Informe se é verdadeiro (V) ou falso (F) o que se afirma a respeito das características de um padrão primário sobre o qual foram feitas as seguintes afirmações:
( ) Deve ter pureza superior a 80%.
( ) Deve ser pouco solúvel no solvente utilizado.
( ) Deve ser de fácil obtenção, dessecação e conservação.
( ) Não pode ser higroscópico, nem reagir com componentes do ar.
( ) Não pode apresentar uma elevada massa molar, facilitando a pesagem.
De acordo com as afirmações, a sequência correta é
Provas
Um técnico de laboratório preparou 100 mL de uma solução de hidróxido de sódio 0,100 mol L-1 para ser utilizada em uma aula prática de quantificação de ácido acético em amostras de vinagre. Antes de utilizar essa solução, ela foi padronizada com hidrogenoftalato de potássio, cuja estrutura está representada a seguir, empregando-se uma massa de 0,204 g desse sal. Ao final do processo, o técnico verificou que a concentração real da solução corresponde a 0,112 mol L-1.
Dado de massas (g mol-1): K= 39, O= 16, C= 12, H=1
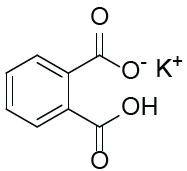
O Estrutura do hidrogenoftalato de potássio
Qual volume aproximado da solução de NaOH, em mL, foi empregado na padronização da solução preparada?
Provas
Os triglicerídeos ou triacilgliceróis são utilizados pelos mamíferos e plantas para armazenamento de energia em longo prazo. Por isso, esses lipídeos desempenham importantes funções biológicas.
Sobre essas substâncias e seus constituintes está correto o que se afirma em:
Provas
O conhecimento sobre as forças intermoleculares nos permite conhecer e explicar diversas propriedades físicas das substâncias.
Nesse contexto, informe se é verdadeiro (V) ou falso (F) o que se afirma a seguir.
( ) A única força intermolecular presente em todas as moléculas e átomos é a força de dispersão, também chamada de força de London.
( ) A ordem de grandeza das forças de dispersão depende da polarizabilidade das moléculas em resposta a um dipolo instantâneo.
( ) A interação intermolecular dipolo permanente é mais intensa em moléculas apolares, que possuem uma maior nuvem eletrônica.
( ) A tensão superficial em substâncias com interações dipolo permanente é menor do que nas substâncias com apenas interações de London.
De acordo com as afirmações, a sequência correta é
Provas
O benzeno é uma substância pouco reativa. Para realizar a bromação do anel aromático, devemos utilizar Br2, na presença de um ácido de Lewis, por exemplo, o cloreto de alumínio, conforme a equação química a seguir:
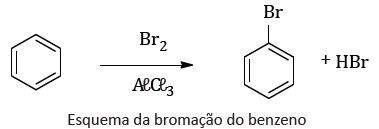
A reação representada é chamada de
Provas
Leia e preencha as lacunas do texto a seguir.
O óxido de cálcio é um sólido de elevada temperatura de fusão que pode ser obtido a partir da decomposição térmica do carbonato de cálcio, cuja fórmula é . Nessa reação também é liberado o gás carbônico. Quando o óxido de cálcio é adicionado em água, forma-se um produto insolúvel, o . Ao gotejar ácido clorídrico nessa suspensão, a solução torna-se incolor devido à formação de um sal , denominado de cálcio.
A sequência que preenche corretamente as lacunas do texto é
Provas
Ao organizar as prateleiras de reagentes de um laboratório, observou-se que o rótulo do frasco de metanoato de metila estava danificado na região que continha a pureza do reagente. Para chegar à pureza aproximada desse reagente e reconstruir o rótulo, em um balão de reação adicionaram-se 120 g do reagente contido no frasco de metanoato de metila. Em seguida realizou-se uma reação de hidrólise, na qual foram produzidas duas substâncias distintas, um ácido carboxílico e um álcool. A massa produzida do álcool foi igual a 25,6 g. Suponha que o rendimento para essa reação realizada foi de 80%.
Dados de massas (g mol-1): O= 16, C= 12, H= 1.
Qual a pureza aproximada, em %, do reagente do frasco de metanoato de metila?
Provas
No processo de recuperação de um metal X presente em uma solução, houve a deposição por galvanização de 200 g desse metal, com elevado grau de pureza. O processo foi realizado empregando-se uma corrente de 30 A, durante 4 horas.
Dados: MMX= 178,5 g mol-1
Constante de Faraday= 96500 C
Qual o número de oxidação do metal X na solução?
Provas
A energia de rede do cloreto de sódio (NaCl) é difícil de ser medida diretamente através de técnicas experimentais. Porém, ela pode ser calculada por meio do conhecimento de outros processos envolvidos na formação desse sólido. Uma forma de calcular esse parâmetro é a partir do ciclo de Born-Haber, uma aplicação da Lei de Hess.
Analise os dados da tabela a seguir.
| Dado | Energia/ (kJ mol-1) |
| !$ \Delta \, H_f \, º !$ Na(g) a partir do Na(s) | +108 |
| Energia de Ionização Na(g) | +494 |
| Energia para dissociar o Cl2(g) | +244 |
| Afinidade Eletrônica Cl(g) | -349 |
| !$ \Delta \, H_f \, º !$NaCl(s) | -412 |
Qual o valor do módulo da energia de rede, em kJ mol-1, do cloreto de sódio?
Provas
Caderno Container