Foram encontradas 919 questões.
Soluções tampão são importantes em diversos estudos, uma vez que o funcionamento apropriado de muitos sistemas depende do pH. Nas alternativas a seguir, aponte o pH de uma solução constituída por KH2PO4, numa concentração de 0,200 mol.L-1 e K2HPO4, sob concentração de 0,100 mol.L-1.
(Dados: pKa do íon H2PO4 − é 7,21; log 2 = 0,3.)
Provas
- Sistemas de EquilíbrioSistemas Heterogêneos: Produto de Solubilidade (Kps)
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Calcular a solubilidade do cromato de prata, Ag2CrO4, em mol.L−1 presente em uma solução de nitrato de prata, AgNO3, 0,010 mol.L-3.
(Dado: Kps = 2,0x10−12)
Provas
Suponha que uma mistura SO2, O2 e SO3 esteja em equilíbrio a 852 K.
2 SO2 (g) + O2 (g) → 2 SO3(g)
As concentrações de equilíbrio são [SO2] = 3,61 x 10-3 mol/L, [O2] = 6,11 x 10-4 mol/L e [SO3] = 1,01 x 10-2 mol/L. Assim sendo, a constante de equilíbrio calculada desse equilíbrio, na temperatura dada, será
Provas
O MTBE (éter-tert-butilmetílico) tem sido usado como aditivo na gasolina. O composto é produzido pela reação do metanol com o isobuteno, de acordo com a seguinte equação:
CH3OH + (CH3)2C=CH2 → (CH3)3COCH3
Se deixarmos 45,0kg de metanol reagir com 70,0kg de isobuteno, assinale a alternativa que apresente a massa em grama de MTBE obtida.
Provas
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
- Química OrgânicaIsomeria Plana e Espacial
Um dos estereoisômeros do 3-bromo-2-butanol pode ser representado conforme sua fórmula em perspectiva a seguir:
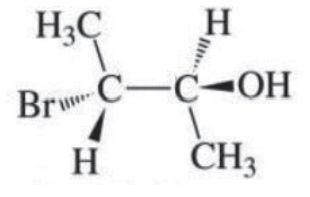
Baseado no sistema de nomenclatura de Cahn-IngoldPrelog, assinale a alternativa que melhor caracterize o nome da representação precedente.
Provas
Na teoria do modelo atômico quântico, as propriedades dos elétrons são especificadas pelos números quânticos. A esse respeito assinale a alternativa correta.
Provas
Como etapa determinante da velocidade de uma reação SN1 é a dissociação do haleto para formar um carbocátion, dois fatores afetam a velocidade de uma reação SN1: a facilidade com que um grupo de saída se dissocia do carbono e a estabilidade do carbocátion que é formado. Em relação às reatividades relativas de haletos de alquila na reação SN1, assinale a alternativa correta.
Provas
A combinação das Leis de Boyle, de Charles e de Avogadro gerou a Lei dos Gases Ideais, representada pela expressão PV = nRT. Essa é uma equação de estado que descreve a resposta de um gás ideal a mudanças de pressão, volume, temperatura e quantidade de moléculas. Entretanto, vários processos industriais e pesquisas em laboratório usam gases sob alta pressão ou em condições muito baixas de temperatura, condições nas quais as leis dos gases ideais não são exatamente respeitadas. Nesses casos, o comportamento se assemelha ao dos gases reais. Em relação à teoria dos gases reais e ideais, afirma-se corretamente que
Provas
A termoquímica é o estudo do calor produzido ou consumido nas reações químicas. É um ramo da termodinâmica, pois o vaso da reação e o seu conteúdo constituem um sistema, e as reações químicas provocam troca de energia entre o sistema e a vizinhança. Sobre a termoquímica é correto afirmar que
Provas
A pilha formada pelos eletrodos que compõem a bateria de chumbo utilizada em automóveis é representada por
Pb(s)| PbSO4(s) | H+(aq), HSO4 −(aq) | PbO2(s) | PbSO4(s) | Pb(s) (E° = 2 V)
Em relação a essa pilha, considere as afirmativas a seguir:
I. Os eletrodos são de metal/metal insolúvel em contato com solução de íons do metal.
II. A reação anódica é Pb(s) + HSO4 −(aq) →PbSO4(s) + H+(aq) + 2e−.
III. Trata-se de uma pilha primária, pois pode ser recarregada.
IV. O Pb contido em baterias gastas não pode ser reciclado devido à presença de H2SO4.
Assinale
Provas
Caderno Container