Foram encontradas 981 questões.
Uma solução padrão é preparada a partir de solutos considerados padrões primários que devem apresentar algumas características específicas, dentre elas:
Provas
Questão presente nas seguintes provas
A ingestão de íons F-1 (aq) diminui a incidência de cáries nas crianças, porém, a ingestão diária de concentrações acima de 0,07 ppm desse íon pode causar uma doença chamada fluorese dental, que, por sua vez, prejudica a dentição infantil. Ao analisar algumas amostras de água mineral, um técnico identificou as seguintes concentrações para esse íon:
| Amostra |
Concentração de íons F-1
(aq) g/dL
|
| I | 4,0 x 10-3 |
| II | 2,5 x 10-5 |
| III | 8,0 x 10-6 |
| IV | 6,0 x 10-7 |
Entre as amostras analisadas, a que se encontra adequada ao consumo diário é a
Provas
Questão presente nas seguintes provas
O seguinte esquema apresenta a separação de alguns polímeros por diferença de densidade.
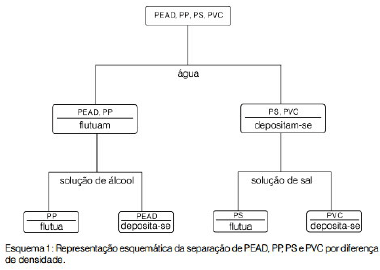
Disponível em: <http://qnesc.sbq.org.br/online/qnesc17/a08.pdf >. Acesso
em: 18 mar. 2013.
Com base nas informações apresentadas no esquema, ao se misturar pequenos pedaços de placas de isopor, seringas de injeção, potes plásticos de sorvete e tubos de encanamento e se realizar os procedimentos indicados, ao final do processo, na solução de sal, flutuarão pedaços de
Provas
Questão presente nas seguintes provas
As estruturas geométricas do dióxido de enxofre, da amônia, do metano e do ácido fluorídrico são, respectivamente:
Provas
Questão presente nas seguintes provas
Na série de íons isoeletrônicos Al+3, Mg+2, Na+1, F-1, O-2 e N-3, o íon que terá maior raio é o
Provas
Questão presente nas seguintes provas
A massa de 3,01 x 1020 moléculas de aspirina é 0,09 g. A composição centesimal da aspirina é: 60% de C (12 g/Mol), 4,44 % de H (1 g/Mol) e 35,56% de O (16 g/Mol). A fórmula molecular desse composto é:
Provas
Questão presente nas seguintes provas
Em uma garrafa fechada de refrigerante, o CO2 dissolvido encontra-se em maior concentração do que em uma garrafa de refrigerante aberta. Tal fato ilustra
Provas
Questão presente nas seguintes provas
A pressão de vapor de equilíbrio de qualquer substância é a medida da tendência das moléculas escaparem da fase líquida e entrarem na fase vapor, em uma dada temperatura.
A partir desse aspecto, quanto maior for a pressão de vapor de equilíbrio, maior será a
Provas
Questão presente nas seguintes provas
A tabela a seguir apresenta pontos de fusão e pontos de ebulição para alguns compostos orgânicos.
| Composto |
Massa molar
(g/Mol)
|
PF (ºC) | PE (ºC) |
| etoxi etano (A) | 74 | - 116 | 34,6 |
| butanol (B) | 74 | - 90 | 117,7 |
Com base nos dados, infere-se que as forças de atração intermoleculares nos dois compostos interferem nos valores de PE e PF. As forças intermoleculares predominantes em A e B são, respectivamente:
Provas
Questão presente nas seguintes provas
A ureia, um dos produtos de excreção do nitrogênio pelo organismo humano, tem fórmula molecular CH4N2O. Esse composto apresenta em sua estrutura o grupo orgânico
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container